Synthèse
de molécules odorantes, concours général
physique chimie 2025.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| . |
.
.
|
|
.
.
|
..
..
......
...
|
Synthèse de l'acétate de 2-phényléthyle.
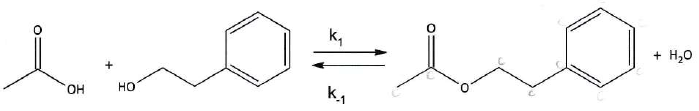
Dans un montage à reflux on introduit 1,5 mol d'acide éthanoïque et 1,5
mol de 2-phényléthanol et quelques gouttes d'acide sulfurique
concentré. On chauffe à 50°C pendant 2 heures.
On verse le contenu du ballon dans un becher contenant une solution
saturée de chlorure de sodium. On sépare les deux phases à l'aide d'une
ampoule à décanter.
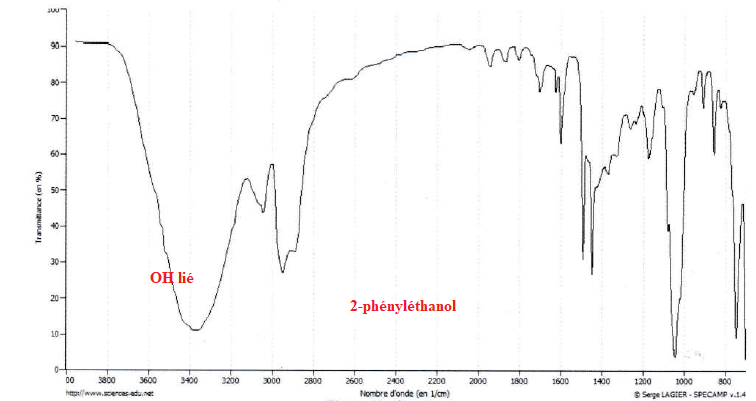
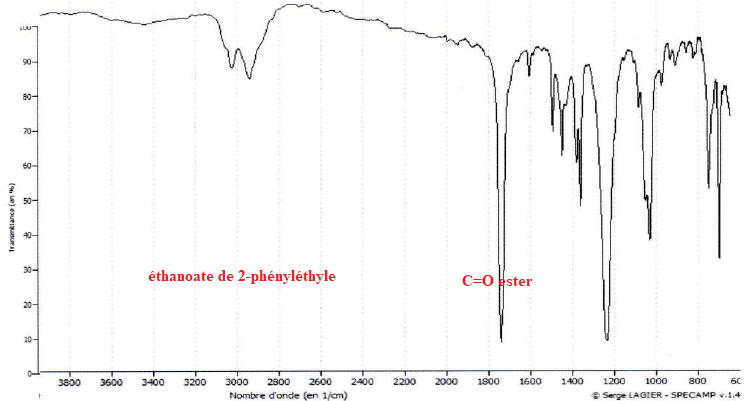
Après distillation de la phase organique on isole deux composés dont on donne les spectres IR.
29. Indiquer les avantages d'un chauffage à reflux.
Il augmente la vitesse d'une réaction lente en travaillant à température modérée.
On évite les pertes de matière : les vapeurs se condensent dans le réfrigérant et retombent dans le ballon.
30. Préciser la famille fonctionnelle de l'acétate de 2-phényléthyle ainsi que son nom en nomenclature officielle.
Famille des esters.
éthanoate de 2-phényléthyle.
31. Attribuer les spectres IR aux molécules citées.
Etude du mécanisme.
32. Indiquer le type de réaction impliqué dans cette synthèse.
Addition ( condensation) d'un alcool sur un acide carboxylique.
33 à 35.
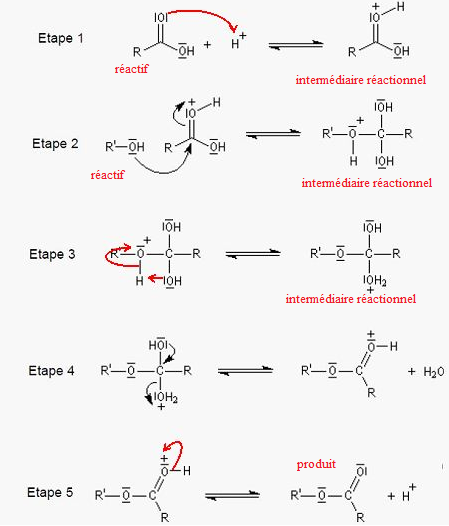
36. Quel est le rôle de l'acide sulfurique ?
Cet acide joue le rôle de catalyseur.
37. Rappeler l'expression du taux d'avancement d'une réaction.
Le taux d'avancement d'une réaction est le rapport de l'avancement à l'état final sur l'avancement maximal de la réaction.
On obtient un taux d'avancement de 66 %.
38. Déterminer le volume d'ester que l'on peut espérer obtenir à l'issue de la transformation.
Quantité de matière d'ester : 0,66 x1,5 = 0,99 mol.
Masse molaire de cet ester : 164 g / mol.
Masse : 0,99 x164 =162,36 g.
Densité d = 1,04.
Volume : 162,36 / 1,04 ~156 mL.
39. Indiquer les conditions initiales ou les conditions de réaction qui permettent d'optimiser cette transformation.
Utiliser un réactif en large excès.
Eliminer l'eau au fur et à mesure de sa formation.
Suivi cinétique de la synthèse par dosage pH-métrique.
On prélève au cours de la réaction un échantillon de 0,5 L du mélange.
On ajoute rapidement 30,0 mL de solution froide d'hydroxyde de sodium à
0,10 mol /L qui réagit totalement avec les acides présents en solution.
On titre l'excès d'hydroxyde de sodium n'ayant pas réagi par une solution d'acide chlorhydrique à 0,1 mol / L.
40. Indiquer pourquoi il est utile de refrodir la solution d'hydroxyde de sodium.
La réaction acide base est exothermique. En refroidissant la solution d'hydroxyde de sodium on réalise un blocage cinétique.
41. Ecrire l'équation de la réaction modélisant cette transformation.
Acide sulfurique : H3O+ aq + HO-aq --> 2H2O(l).
Acide éthanoïque : CH3-COOH aq +HO-aq --> CH3-COO-aq +H2O(l).
42. Ecrire l'équation de support du dosage.
H3O+ aq + HO-aq --> 2H2O(l).
On considère que le volume prélevé est négligeable par rapport au volume du mélange réactionnel.
43. Déterminer le volume équivalent.
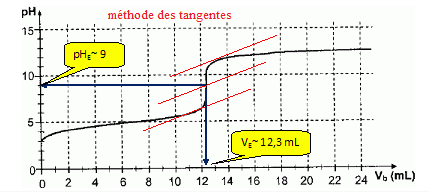
44. Donner deux
hypothèses expliquant qu'avec cette démarche de dosage on obtienne un
taux d'avancement légérement inférieur à 66 %.
L'hydroxyde de sodium réagit également avec l'acide sulfurique ainsi qu'avec l'ester. ( hydrolyse basique de l'ester).
45. Estimer la quantité d'acétate de phényléthyle formé.
Quantité de matière maximale d'ester : 1,5 x0,66 = 0,99 mol.
|
...
|
....
|
Etude cinétique de la réaction.
On va estimer si la cinétique globale de cette réaction peut être assimilée à une vitesse d'ordre 1.
La réaction étant équimolaire pour les deux réactifs et sans présence
de produits à l'atat initial, l'étude peut être simplifiée en
considérant l'unique équation suivante avec une constante de réaction k
dans le sens direct et k-1 dans le sens inverse.
A représente les deux réactifs et B les deux produits.
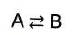
Les réactifs et produits sont liquides.
On note nA et nB les quantités de matière respectives de A et de , et Vtot le volume total constant du mélange réactionnel.
Considérons une quantité initiale nA i de 1,5 mol de A et nB i = 0 mol de B.
46 Définir la vitesse volumique de la réaction.
v = -d [A] /dt = d[B] / dt.
47. Montrer qu'on arrive à l'équation différenteille suivante.
dnA/dt = -k1nA +k-1nB.
Le volume étant constant et l'ordre étant égal à 1 pour l'équation directe et l'équation indirecte :
dnA/dt = -k1nA +k-1nB.
48. Exprimer cette équation en fonction de l'avancement x de la réaction et des quantités initiales.
nA = na i-x ; nB = x.
dnA/dt = -dx /dt ;
-dx/dt = -k1(nA i -x)+k-1 x.
dx/dt =k1(nA i -x)-k-1 x.
dx /dt =-( k1+k-1)x +k1 nA i .
dx/dt +( k1+k-1)x =k1 nA i .(E).
A l'équilibre la réaction n'évolue plus, on pose x = xe.
49. Exprimer xe en fonction de k1 et k-1. Montrer que la solution de cette équation est :
x(t) = xe(1-exp[-(k1+k-1)t]).
dxe/dt =0 ; ( k1+k-1)xe =k1 nA i ; xe =k1 nA i / ( k1+k-1).
Solution générale de dx/dt +( k1+k-1)x =0.
x (t) = A exp[-(k1+k-1)t] avec A une constante.
Solution générale de (E) :
x (t) = A exp[-(k1+k-1)t]+xe.
x(t=0)=0=A+xe ; A = -xe.
x(t) = xe (1-exp[-(k1+k-1)t] ).
La constante d'équilibre de cette réaction s'écrit K = nB éq / nA eq = 4.
50. Vérifier que k1 = 4k-1.
nA éq =nA i -xeq ; nB eq =xeq ;
K = xeq / (nA i -xeq)=4.
xeq =4(nA i -xeq) ; 5xeq =4 nA i ;
5k1 nA i / ( k1+k-1) =4nA i ;
5k1 =4(k1+k-1 ); k1=4k-1.
.51. Montrer qu'à partir de la solution de cette équation différentielle, le tracé de y = ln(1-x/xe) permet de vérifier si la réaction suit cette cinétique. Tracer son allure et conclure.
x(t) / xe=1-exp[-(k1+k-1)t].
1-x(t) / xe=exp[-(k1+k-1)t].
ln(x(t) / xe)=-(k1+k-1)t.
y = -5k-1 t, droite de pente -5k-1 passant par l'origine.
Reproduire une synthèse naturelle.
Un test d'estérification est réalisé en utilisant des bactéries MsAcT
dans l'eau à 40°C en présence d'une solution tampon selon deux
protocoles : un premier où l'on ajoute MsAct diluée dans l'eau et un
second où MsAct est fixée sur un support solide insoluble dans l'eau.
52. Qualifier les types de catalyses.
Premier protocole : catalyse homogène.
Second protocole : catalyse hétérogène.
La vitesse initiale de réaction est repportée en fonction des quantités
d'alcool ajoutées pour les deux protocoles. Le taux d'avancement final
est de 60 % dans les deux cas. La concentration en anhydride acétique
est fixée à 100 mmol /L.
53 Comparer les vitesses initiales du mélange équimolaire avec celles de la partie 2.1.
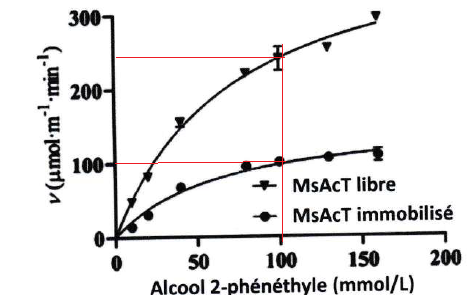
54. Indiquer les quantités optimales et les conditions à privilégier.
Anhydride acétique
est fixée à 100 mmol /L.
Alcool 2-phénéthyle : 150 mmol / L.
Bactéries MsAcT
dans l'eau à 40°C en présence d'une solution tampon.
55. Identifier au moins deux principes de la chimie verte respectés dans cette synthèse.
La synthèse s'effectue dans des conditions de température et de pression ambiante.
Utilisation d'agents catalytiques.
Plusieurs essais sont réalisés en modifiant le deuxième réactif afin
d'obtenir toujours le même ester. On fait réagir l'alcool
2-phényléthyle avec de l'acétate d'éthyle, de l'acétate de vinyle ou de
l'anhydride acétique en présence de MsAcT fixée sur le gel.
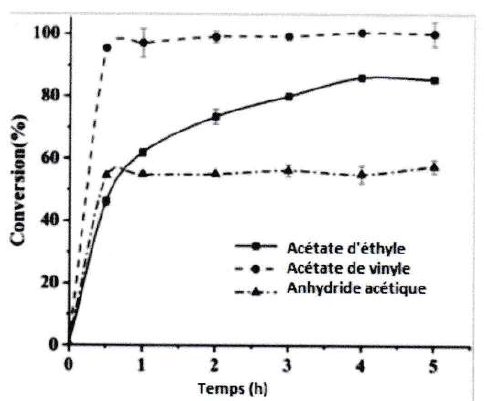
56. Commenter les résultats.
En utilisant l'acétate de vinyle la conversion est de 100 % au bout d'une demi-heure.
|
|
=
|
|