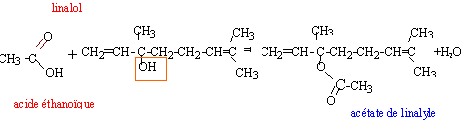|
Concours ESSA Lyon 2010 : de l'huile d'olive au savon parfumé. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts. |
|||||||||||||||
| .
. |
|||||||||||||||
|
|||||||||||||||
|
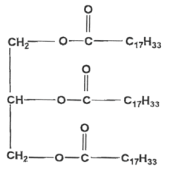
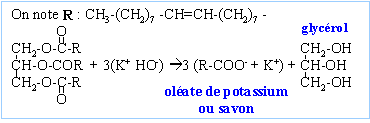
Une huile alimentaire est un mélange complexe de triglycérides qui sont des triesters du glycérol (ou propan-1,2,3-triol) et d'acides gras ; les acides gras majeurs présentent 12 à 18 atomes de carbone. Les savons
:
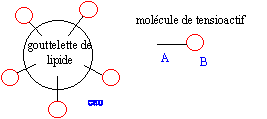
Le savon présente une partie
lipophile et une partie lipophobe. ions carboxylate sur une tache de graisse (lipide) : Ecrire l'équation bilan de la réaction qui traduit ce phénomène de précipitation. Ca2+ aq + 2 C17H33-CO2-aq = Ca(C17H33-CO2-)2 (s). Le savon parfumé à la lavande : Le parfum à odeur de lavande, ou acétate de linalyle, utilisé pour parfumer un savon est une espèce chimique présente dans l'essence naturelle de lavande. Mais il peut aussi être préparé au laboratoire, entre autres par action de l'acide acétique sur le linalol. À température ordinaire, le linalol se présente sous la forme d'un liquide incolore et odorant. Formule semi-développée du linalol : 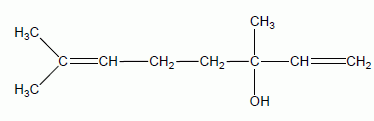 Températures d'ébullition à pression atmosphérique :
L'acétate de linalyle est un ester ; le linalol est un alcool. En utilisant les formules semi-développées, écrire l'équation de la réaction correspondant à la préparation de l'acétate de linalyle.
Quelles sont les caractéristiques de cette réaction ? L'estérification est lente, athermique, limitée par l'hydrolyse de l'ester.
On chauffe à reflux un mélange équimolaire de linalol et d'acide acétique en présence d'un catalyseur. Le rendement de la synthèse, de l'ordre de 5%, est mauvais. Proposer deux méthodes pour améliorer le rendement, sans changer la nature des réactifs, sachant que le linalol est un produit très coûteux ? Eliminer l'un des produits ( le plus volatil : l'eau ) par distillation au fur et à mesure de sa formation. Utiliser le réactif le moins couteux, l'acide acétique, en grand excès. Que proposeriez-vous pour améliorer le rendement, en changeant l'un des réactifs ? Nommer ce nouveau réactif après avoir proposé sa formule semi-développée. Remplacer l'acide acétique par l'anhydride acétique anhydre. 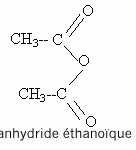
|
|||||||||||||||
| |
|||||||||||||||
|
|