|
Enantiomères, protection d'un diol, phosphite de triéthyle : concours Capes 2012. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts. |
||||
| .
. |
||||
|
||||
|
Formation du composé 10. 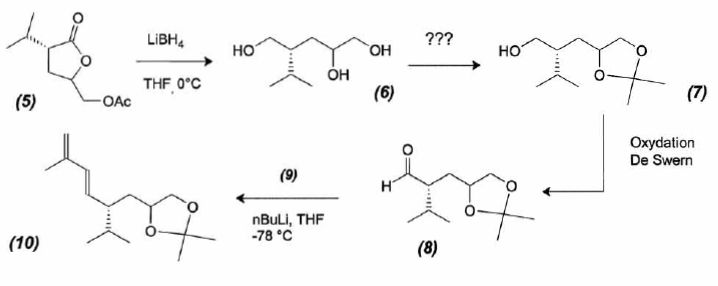 Quel type de réaction réalise t-on avec LiBH4 ? On réalise des réductions : aldehyde, cétone, ester, chlorure d'acyle sont réduits en alcool ; les lactones conduisent à des diols. Proposer un réactif et des conditions opératoires pour raliser la transformetion (6) ---> (7). Quel est le nom donné à cette réaction ? Proposer un mécanisme réactionnel. Le diol est protégé par la formation d’un acétal cylique en utilisant la propanone en présence d'un catalyseur ( acide paratoluènesulfonique). 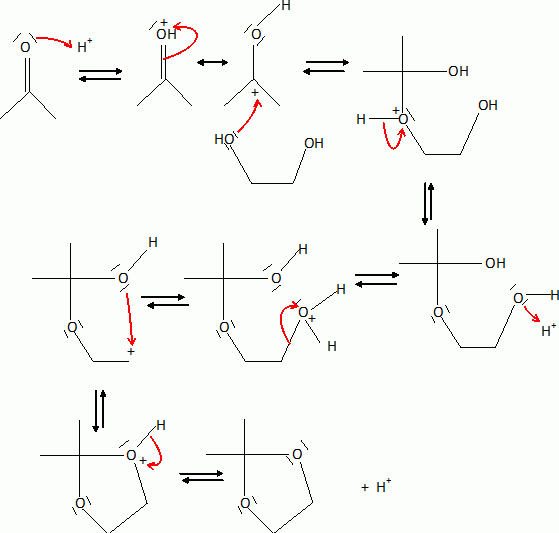
Le composé (7) est oxydé dans des conditions douces ( Swern ) pour donner l'aldehyde (8). Donner la formule topologique du produit que l'on obtiendrait si on utilisait un oxydant fort ( K2Cr2O7 par exemple ). 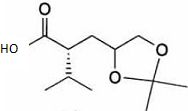 De plus en milieu acide, on risque d'hydrolyser l'acétal cyclique. Le réactif (9) est préparé par action du phosphite de triéthyle ( P(OEt)3) sur le 3-chloro-2-méthylprop-1-ène. A l'aide du schéma de Lewis de P(OEt)3, justifier la nucléophilie du phosphite de triéthyle. En déduire la formule topologique du cation (9). Grâce au doublet libre présent sur l'atome de phosphore, le phosphite de triéthyle est un composé très nucléophile. Le phosphite de triéthyle et un halogénure d’alkyle réagissent selon un mécanisme de substitution nucléophile SN2. L'action du buthyllithium sur (9) donne un composé (9'). Réaction d'Arbuzov. 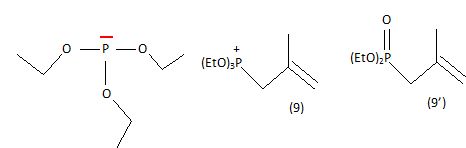 A quelle réaction classique, le passage de (8) à (10) peut-il s'apparenter ? Réaction de Wittig : action d'un ylure de phosphore sur un dérivé carbonylé.
|
||||
|
|