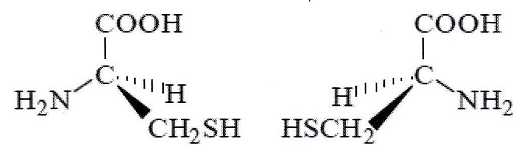|
|
|
|
Titrage
pH-mťtrique.
A)
Lors du titrage pH-mťtrique d'un acide faible par une base forte, le pH
du milieu rťactionnel ŗ la demi-ťquivalence est ťgal ŗ la moitiť du pH
ŗ l'ťquivalence. Faux.
A la
demi-ťquivalence de ce titrage, le pH est ťgal au pKa
du couple acide faible / base conjuguťe.
B) Lors du titrage pH-mťtrique d'un acide fort par une base forte, ŗ
l'ťquilibre le pH vaut 7 ŗ 25 įC. Faux.
A
l'ťquivalence de ce titrage, le pH vaut 7 ŗ 25 įC.
C)
Lorsque les rťactifs sont introduits en proportions stoechimťtriques de
l'ťquation chimique de la rťaction support du titrage pH-mťtrique, le
pH dťpend de la tempťrature du milieu rťactionnel. Vrai.
Le pH dťpend
de la tempťrature.
D)
Lors du titrage pH-mťtrique d'une base forte par un acide fort, on peut
ťcrire, ŗ l'ťquivalence du titrage : pH = ĹpKe.
Vrai.
E)
Lors du dosage par titrage pH-mťtrique, il convient d'utiliser un
indicateur colorť de pH pour repťrer l'ťquivalence, gr‚ce au changement
de couleur du milieu rťactionnel. Faux.
Le
changement de couleur d'un indicateur colorť permet de repťrer
l'ťquivalence lors d'un dosage colorimťtrique.
Question
2.
Soit la rťaction d'ťquation CH3COOH aq +HO-aq
---> CH3COO-aq + H2O(l).
A) La constante d'aciditť du couple acide ťthanoÔque / ion ťthanoate
s'ťcrit :
Ka = [CH3COO-aq] /([CH3COOH aq][HO-aq]). Faux.
Ka = [CH3COO-aq][H3O+aq]
/([CH3COOH aq].
B) L'acide ťthanoÔque possŤde un
groupe caractťristique acide carboxylique. Vrai.
C) L'acide
ťthanoÔque ne possŤde pas de carbone tťtraŤdrique. Faux.
Le
carbone du groupe CH3- est tťtraŤdrique.
D)
Le dosage d'une solution d'acide ťthanoÔque par une solution
d'hydroxyde de sodium peut aussi Ítre rťalisť par titrage pH-mťtrique
que colorimťtrique ou conductimťtrique. Vrai.
On mťlange 50,0 mL d'une solution d'acide ťthanoÔque de concentration ca
= 1,0 10-2 mol/L avec 25,0 mL d'une solution
aqueuse d'hydroxyde de sodium de mÍme concentration apportťe.
E) La solution obtenue est une
solution tampon de pH. Vrai.
On
se trouve ŗ la demi-ťquivalence d'un dosage acide faible base forte, le
pH est ťgal au pKa du couple cide faible / base
conjuguťe.
Question
3.
A) La reprťsentation de Lewis d'une molťcule permet la visualisation
dans l'espace decette molťcule. Faux.
La
reprťsentation de Lewis met en ťvidence les liaisons et les doublets
non liants.
B) La molťcule de 1-bromo-1-chloroťthane ne possŤde pas de carbone
asymťtrique. Faux.
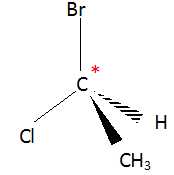
C) Il est possible de passer d'une conformation d'une molťcule ŗ une
autre par rupture de liaisons simples. Faux.
On passe
d'une conformation ŗ une autre par rotation autour d'une liaison simple.
D) Un mťlange racťmique est un mťlange de deux diastťrťoisomŤres. Faux.
Un mťlange
racťmique est constituť de deux ťnantiomŤres en proportions identiques.
E) Deux ťnantiomŤres rťagissent diffťremment avec des rťactifs chiraux.
Faux.
Deux
ťnantiomŤres ont les mÍmes propriťtťs chimiques.
|
.
|
Dissolution
du chlorure de cuivre (II).
Le chlorure de cuivre (II) est trŤs soluble dans l'eau. A 25įC on peut
disoudre 700 g de ce cristal ionique anhydre dans un litre d'eau. Une
solution de cuivre (II) a une concentration en ion chlorure ťgale ŗ
20,0 mmol/L. Sa concentration en ions cuivre (II) est :
A) 10 mmol/L. Vrai.
La solution
est ťlectriquement neutre [Cl-] = 2 [Cu2+]
; [Cu2+]
= 20 / 2 = 10 mmol / L.
B) 40 mmol / L. Faux.
On veut prťparer une solution de concentration [Cu2+aq]
= 20,0 mmol/L avec des cristaux de chlorure de cuivre (II), solide
hydratť de formule CuCl2, 2H2O.
Donnťe : M(CuCl2) = 134,5 g/ mol. La masse de
solide ŗ dissoudre pour obtenir 100 mL de solution est :
C)
0,341 g. Vrai.
Quantitť de
matiŤre de solutť = quantitť de matiŤre d'ion cuivre (II) = 20,0 10-3
*0,100 =2,00 10-3 mol.
M(CuCl2, 2H2O)
= 134,5 +36 = 170,5 g/mol.
Masse de
solutť : 2,00 10-3 *170,5 =0,341 g.
D) 0,269 g. Faux.
E) On utilise un bťcher graduť de 250
mL pour fabriquer cette solution. Faux.
On utilise une
fiole jaugťe de 100,0 mL.
Acides
a-aminťs.
Les acides a-aminťs
sont des constituants des protťines. Ils ont pour formule gťnťrale : H2N-CHR-COOH.
A) Ces molťcules possŤdent deux groupes caractťristiques : le groupe
amine et le groupe acide carboxylique. Vrai.
B) Les acides a-aminťs
possŤdent un caractŤre amphotŤre. Vrai.
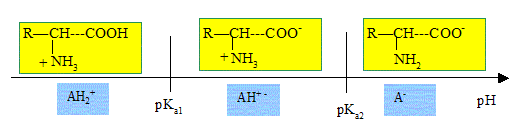
Le pH isoťlectrique correspond
ŗ une valeur particuliŤre du pH d'une solution d'acide aminť. A cette valeur du pH la solution
possŤde un caractŤre amphotŤre.
La
kťratine est le principal constituant du cheveu. C'est une protŤine
formťe ŗ partir d'acides a-aminťs dont l'un d'eux est la cystťine de
formule :
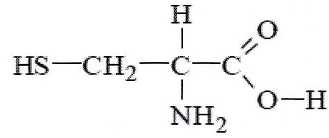
C) La cystťine est une molťcule
achirale. Faux.
Cette
molťcule possŤde un atome de carbone asymťtrique.
D) Les reprťsentations de Cram suivantes sont celles de deux
ťnantiomŤres de la cystťine. Vrai.
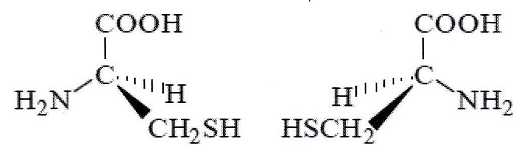
E)
La cystťine possŤde un atome de carbone de gťomťtrie plane. Vrai.
L'atome de
carbone du groupe carboxyle.
|
|
Les ions iodures I- sont oxydťs lentement par les ions peroxodisulfate S2O82-.
On peut ťtudier expťrimentalement la cinťtique de cette rťaction en
dosant rťguliŤrement le diiode formť, ce qui permet de tracer la courbe
[S2O82-aq] = f(t), donnant en fonction
du temps la concentration en ions peroxodisulfate restants. Une
premiŤre expťrience, rťalisťe en prťsence d'ion Fe3+aq catalyseur ŗ la tempťrature q1, permet de tracer la courbe ci-aprŤs.
A) La catalyse par les ions Fe3+aq est hťtťrogŤne. Faux.
Catalyseur et rťactifs sont dans la mÍme phase : la catalyse est homogŤne.
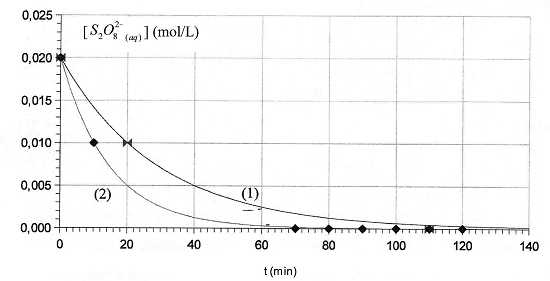
B) A t1 = 60 minutes, la concentration en diiode dans la solution est de 1,8 10-2 mol/L. Vrai.
[S2O82-aq]60 =2,0 10-3 mol/L d'aprŤs le graphe (1).
S2O82-aq + 2I-aq --> 2 SO42-aq + I2aq. [S2O82-aq]0 - [S2O82-aq]60 =[I2aq]60 =0,02 -2,0 10-3=0,018 mol/L.
On recommence la mÍme expťrience ŗ une tempťrature q2 diffťrente et on obtient la courbe (2).
C) q2 > q1. Vrai.
Le temps de demi rťaction tĹ(2) = 10 min est infťrieur ŗ tĹ(1) =20 min.
D) q2 < q1. Faux.
E) La tempťrature du milieu rťactionnel est un catalyseur de la rťaction ťtudiťe. Faux.
La tempťrature est un facteur cinťtique.
|
|