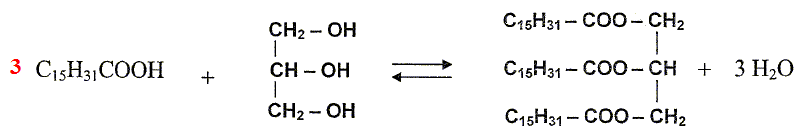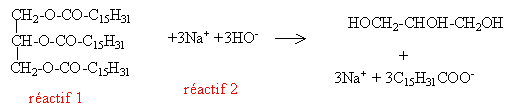|
|
|
|
Accumullateur.
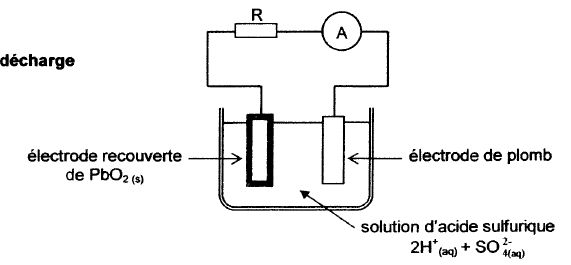
La batterie d'une voiture est constituťe de plusieurs
accumulateurs au plomb. Chacun d'entre eux comprend deux ťlectrodes :
l'une est en plomb, l'autre est recouverte de dioxyde de plomb PbO2(s).
Elles sont plongťes dans une solution aqueuse d'acide sulfurique 2H+aq
+ SO42-aq.
Les couples oxydant / rťducteur sont : PbO2(s) /
Pb2+aq et Pb2+aq
/Pb(s).
M(Pb) = 207,2 g/mol ; 1 F = 96500 C mol-1 ; NA =
6,02 1023 mol-1 ; e = 1,6 10-19 C.
Ecrire l'ťquation
et prťciser la nature ( rťduction ou oxydation ) de la rťaction se
produisant au niveau de chaque ťlectrode.
Oxydation ŗ l'anode nťgative : Pb(s) = Pb2+ aq + 2e-.
Rťduction ŗ la cathode positive : PbO2(s) + 2e-+
4H+aq = Pb2+
aq +2H2O.
Bilan : PbO2(s) +4H+aq + Pb(s) = 2 Pb2+
aq +2H2O.
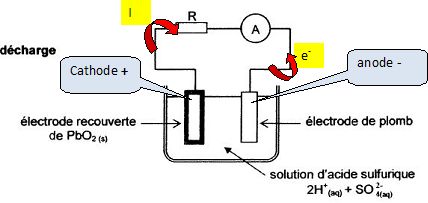
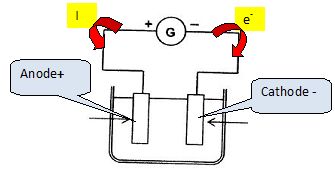
Indiquer
sur le schťma les deux ťlectrodes, le sens de circulation du courant et
des ťlectrons dans le circuit.
La charge maximale d'un
accumulateur est 2 105 C.
Calculer
la masse de plomb consommťe s'il se dťcharge complŤtement.
Quantitť de matiŤre d'ťlectron : 2 105 / 96500 = 2,07 mol.
n(Pb) = Ĺn(e- ) = 1,036 mol.
Masse de plomb : M(Pb) n(Pb) = 207,2 *1,036 = 214,7 ~215 g.
Cet accumulateur va Ítre
rechargť ŗ l'aide d'un gťnťrateur G de courant continu d'intensitť
ťgale ŗ 4 A. Il fonctionne comme un ťlectrolyseur.
Ecrire
l'ťquation bilan de la charge de la batterie.
2 Pb2+
aq +2H2O =PbO2(s) +4H+aq + Pb(s).
Indiquer sur le schťma les deux ťlectrodes, le sens de circulation du
courant et des ťlectrons dans le circuit.
Quelle
est la durťe de la charge complŤte ?
Q = I t ; t = Q / I = 2 105 / 4 = 5 104 s ( ~ 14 heures ).
|
.
|
Acide sulfamique.
L'acide sulfamique H2NSO3H est utilisť comme
dťtartrant pour cafetiŤre. Il est vendu sous forme de poudre blanche
que l'on souhaite titrer afin d'en connaÓtre le pourcentage en acide.
Pour cela on dissout 0,5 g de ce dťtartrant dans 100 mL d'eau distillťe
( solution S). On ajoute progressivement ŗ cette solution un volume vb
d'une solution aqueuse d'hydroxyde de sodium de concentration cb
= 0,3 mol/L. La courbe ci-dessous indique les variations du pH de la
solution au cours du titrage.
Ecrire
l'ťquation de la rťaction de titrage.
H2NSO3H aq + HO-aq = H2NSO3-aq
+ H2O(l).
Dťterminer
les coordonnťes du point ťquivalent. La courbe pH = f(vb)
permet-elle de dťterminer si l'acide sulfamique est un acide fortou
faible ? Justifier.
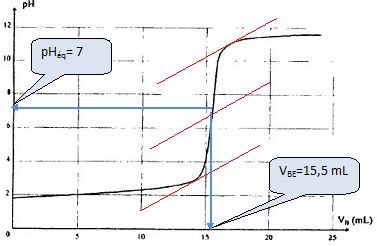
L'allure de la courbe pour vb =0 et pHťqui
~7 indiquent que l'acide sulfamique est un acide fort.
Quelle
est la concentration cA de la solution S ?
A l'ťquivalence cA Va = cb vBE
; cA = cb vBE / Va = 0,3
*15,5 / 100 =4,65 10-2 ~4,7
10-2 mol/L.
Calculer
la masse d'acide prťsent dans la solution S. En dťduire le pourcentage
d'acide sulfamique dans ce dťtartrant.
M(acide sulfamique) = m = 2+14 +32+3*16+1 =97 g/mol.
m = M n = 97 *4,65 10-3 ~0,45
g soit 0,45 / 0,50 *100 = 90 %.
|
Savon.
L'acide
palmitique est un acide gras saturť prťsent dans l'huile de palme mais
aussi dans toutes les graisses et huiles animales ou vťgťtales (
beurre, fromage, lait et viande ). Sa formule semi-dťveloppťe est
donnťe.
Nommer et entourer le groupe caractťristique de cette molťcule.
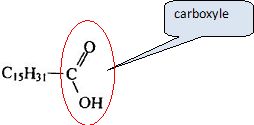
L'huile de palme contient aussi de la palmitine, triester du glycťrol HOCH2-CH(OH)-CH2OH et de l'acide palmitique.
Ecrire l'ťquation de la rťaction de synthŤse de la palmitine.
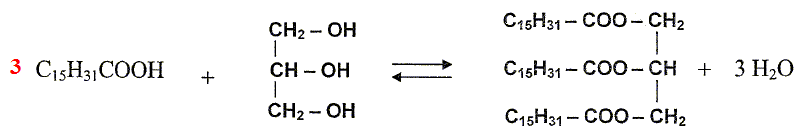
L'huile de palme est trŤs utilisťe dans la fabrication de savon obtenu par action ŗ chaud d'une solution d'hydroxyde de sodium.
Quel
est le composant de l'huile de palme qui rťagit avec l'hydroxyde de
sodium pour donner du savon ? Ecrire l'ťquation de cette saponification
et nommer les produits obtenus.
Palmitine + 3 hydroxyde de sodium = 3 palmitate de sodium + glycťrol.
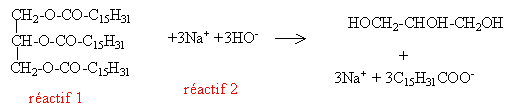
|
|