QCM
de chimie.
Concours kinť EFOM 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
.
|
|
|
|
|
|
|
Oxydation du propan-2-ol par les ions permanganate en milieu acide.
On mťlange un volume V = 7,7 mL de propan-2-ol pur et 0,050 mol d'ion permanganate MnO4- en milieu acide
L'ťquation de la raction est : 5C3H8O +2MnO4- +6H+ --> 5C3H6O +2Mn2++8H2O.
Densitť par rapport ŗ l'eau du propan-2-ol d = 0,78.
Aide aux calculs : 7,7 / 7,8 ~7,8 / 7,7 ~1 ; 7,8 *7,7 ~60.
A. L'alcool utilisť est primaire. Faux.
C'est un alcool secondaire.
B. La masse molaire du propan-2-ol est M = 60,0 g/mol . Vrai.
M = 12*3 +8+16 =60 g/mol.
C.
Le produit de l'oxydation est le propanal. Faux.
Le produit de l'oxydation est la propanone ou acťtone.
D. Le mťlange initial est tel que l'alcool est le rťactif limitant. Vrai.
Quantitťs de matiŤre initiales : n(alcool) =V d / M =7,7*0,78 / 60 =6/60 = 0,1 mol ;
0,1 mol d'alcool ragit avec 0,1 /2,5 = 0,04 mol d'ion permanganate ; ce dernier est en excŤs.
E.
La transformation est catalysťe par les ions H+. Faux.
Les ions H+ sont l'un des rťactifs.
Solution d'ion fer (II).
On souhaite prťparer, ŗ partir du sel de Mohr FeSO4, (NH4)2SO4, 6H2O, un volume Vsol = 50 mL d'une solution aqueuse de concentration molaire effecttive en ion Fe2+ ťgale ŗ c=0,20 mol/L. Masse molaire du sel de Mohr M = 392,1 g/mol.
A. Il faut peser 3,921 mg de solide. Faux.
n(Fe2+) = Vsol c =0,050 *0,20 =0,01 mol.
Masse ŗ peser : 0,01*392,1 = 3,921 g.
B. Il faut peser 3,921 g de solide. Vrai.
C. Il faut utiliser une pipette jaugťe lors de cette prťparation. Faux.
D. Il faut utiliser une fiole jaugťe lors de cette prťparation.Vrai.
E. AprŤs dissolution complŤte, la concentration en ion sulfate est 0,20 mol/L. Faux.
2*0,20 = 0,40 mol/L.
(FeSO4, (NH4)2SO4, 6H2O)s --> Fe2+aq +2NH4+aq + 2SO42-aq.
Combustion.
La formule semi-dťveloppťe de la 1-hydroxybutan-2-one est 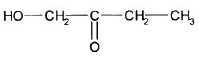
A. L'acide butanoÔque et la 1-hydroxybutan-2-one sont isomŤres. Vrai.
CH3-CH2-CH2-COOH.
B. L'oxydation mťnagťe de la butanone permet d'obtenir l'acide butanoÔque. Faux.
Une cťtone ne subit pas d'oxydation mťnagťe.
La combustion complŤte d'une mole de 2-mťthylpropane en prťsence d'un excŤs de dioxygŤne libŤre :
C. 3 moles de dioxyde de carbone Faux. C4H10 + 6,5O2 --> 4 CO2 + 5 H2O.
D. 5 moles d'eau. Vrai.
E. Le 2-mťthylpropane ne compote que des liaisons simples. Vrai.
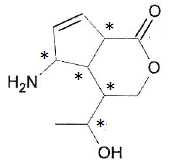
A. La reprťsentation utilisťe est une reprťsentation topologique. Vrai.
B. La formule brute de la molťcule est C10H15O3N. Vrai.
C. La molťcule possŤde un groupe carbonyle. Faux.
La molťcule possŤde un groupe ester cyclique.
D. La molťcule possŤde un groupe hydroxyle. Vrai.
E. La molťcule possŤde 5 atomes de carbone asymťtriques. Vrai.
|
|
|
RMN du proton.
On rťalise le spectre RMN du proton d'une molťcule de formule brute C5H10O2.
Le
spectre fait apparaÓtre 2 triplets et 2 singulets. Chacun des triplets
intŤgre pour 2 protons et chacun des singulets intŤgre pour 3 protons.
A. La molťcule est l'acide pentanoÔque. Faux.
B.
La molťcule est l'ťthanoate de propyle. Faux.
C. La molťcule est le propanoate d'ťthyle. Faux
D. La formule semi-dťveloppťe de la molťcule est : 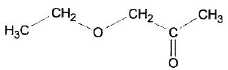 Faux. Faux.
E. La formule semi-dťveloppťe de la molťcule est :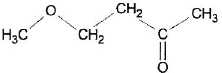 Vrai.
Vrai.
|
.
|
|
Spectrophotomťtrie.
En
vue de rťaliser un suivi cinťtique par spectrophotomťtrie, on mesure
l'absorbance A de diverse solutions aqueuses de diiode de
concentrations diverses.
| [I2] mol m-3 | 0,20 | 0,45 | 0,60 | 1,2 | | [I2] mol L-1 | 0,20 10-3 | 0,45 10-3 | 0,60 10-3 | 1,2 10-3 | | A | 0,2 | 0,45 | 0,6 | 1,2 | | k=A/[I2] en L mol-1. | 1,0 103 | 1,0 103 | 1,0 103 | 1,0 103 |
On fait rťagir une solution aqueuse de peroxyde d'hydrogŤne H2O2 avec des ions iodure I-.
Le peroxyde d'hydrogŤne est en excŤs dans le mťlange. Il se forme du
diiode qui est la seule espŤce colorťe du mťlange. AprŤs agitation
initiale, on place rapidement un ťchantillon du mťlange rťactionnel
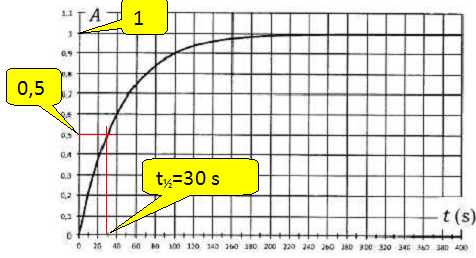
dans le spectrophotomŤtre. La courbe A = f(t) est donnťe ci-aprŤs. La
transformation est supposťe totale.
A. La loi de Beer-Lambert s'exprime ici par A = k [I2] avec k=1,0 10-3 L mol-1. Faux.
B. Les ions iodures subissent une rťduction. Faux.
Oxydation 2I -aq --> I2 aq + 2e-.
C. Le temps de demi-rťaction est environ 30 s. Vrai.
Durťe au bout de laquelle l'avancement est ťgal ŗ la moitiť de l'avancement final.
D. La concentration initiale des ions iodures ťtait 1,0 mol m-3. Faux.
[I2]final = 1 mol m-3 ; [I -]initiale = 2 mol m-3 .
E. Le temps de demi-rťaction serait plus court en chauffant le mťlange. Vrai.
Titrage de l'acide benzoÔque.
A 25įC, le pKa du couple de l'acide benzoÔque C6H5-COOH /C6H5-COO- vaut 4,2. L'ion hydroxyde HO-
est une base forte en solution aqueuse. On rťalise le titrage d'un
volume V =10,0 mL d'une solution aqueuse d'acide benzoÔque par une
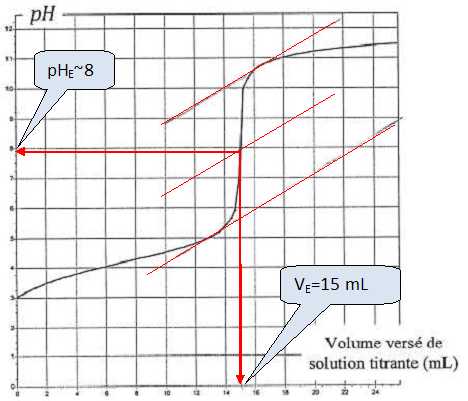
solution d'hydroxyde de sodium ( Na+ +HO-) de concentration molaire c = 1,0 10-2 mol/L. On donne la courbe de suivi-pHmťtrique.
A. Un acide est une espŤce capable de cťder un ou plusieurs ťlectrons. Faux.
Un acide est une espŤce susceptible de cťder un proton.
B. La solution titrante a un pH ťgal ŗ 11,5. Faux.
pH=14 + log c = 14 + log(1,0 10-2) = 12.
C. A l'ťquivalence, le mťlange a le mÍme pH qu'une eau neutre ŗ 25įC.
pHE ~8 (voir graphe).
D. L'ion benzoate prťdomine devant son acide conjuguť dans le mťlange ŗ l'ťquivalence. Vrai.
A pH > pKa, la base conjuguťe prťdomine.
E. La concentration molaire en solutť apportť de lasolution d'acide benzoÔque vaut 1,5 10-2 mol/L. Vrai.
A l'ťquivalence [C6H5-COOH] V = c VE ; [C6H5-COOH] =VE c/V =15*1,0 10-2 / 10 =1,5 10-2 mol/L.
Mťcanisme rťactionnel.
Lors d'une ťtape d'un mťcanisme rťactionnel, les ions cyanure 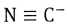 rťagissent avec le mťthanal H2C=O pour former NC-CH2-O-. rťagissent avec le mťthanal H2C=O pour former NC-CH2-O-.
A. Les ions cyanure sont des anions. Vrai.
B. L'atome de carbone du mťthanal est un site donneur de doublet d'ťlectrons. Faux.
C. Les liaisons multiples sont des sites donneurs de doublet d'ťlectrons. Vrai.
D. Cette ťtape est une rťaction de substitution. Faux.
Addition sur le carbone du carbonyle.
E. Lors de cette ťtape, l'atome de carbone de l'ion cyanure est le cite donneur de doublets d'ťlectrons. Vrai.
|
|
|
SynthŤse du mťthanoate d'ťthyle.
| Formule | Densitť | Solubilitť dans l'eau | Tempťrature d'ťbullition įC | | acide mťthanoÔque | HCOOH | 1,22 | trŤs ťlevťe | 100,7 | | ťthanol | CH3-CH2-OH | 0,79 | trŤs ťlevťe | 78,5 | | mťthanoate d'ťthyle | HCOOCH2-CH3 | 0,91 | trŤs faible | 54,3 | | eau | H2O | 1,00 | xxxx | 100 |
La
rťaction entre lacide mťthanoÔque et l'ťthanol produit du mťthanoate
d'ťthyle et de l'eau selon une ťquation de rťaction oý tous les
coefficients stoechiomťtriques sont ťgaux ŗ 1. Dans un ballon on
introduit 2,0 mol d'acide mťthanoÔque, 2,0 mol d'ťthanol , un peu
d'acide sulfurique et quelques grains de pierre ponce. On porte ŗ
ťbullition le mťlange rťactionnel avec un montage ŗ reflux. On rťalise
par la suite un relargage puis une dťcantation. On obtient 0,8 mol
d'ester.
A. Dans ce montage le ballon doit Íte surmontť d'un rťfrigťrant vertical. Vrai.
B. Le mťlange initial est stoechiomťtrique. Vrai.
C. Une distillation fractionnťe permet d'extraire l'ester du mťlange. Vrai.
L'ester est l'espŤce la plus volatil.
D. Lors de la dťcantation du distillat traitť, la phase organique se place sous la phase aqueuse. Faux.
La phase organique est constituťe de l'ester, moins dense que l'eau.
E. Le rendement de la synthŤse est de 80 %. Faux.
rendement = avancement final / avancement maximal = 0,8 / 2 = 0,4 ( 40 %). 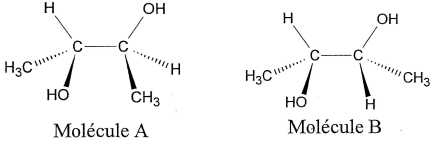
A. La molťcule A possŤde 2 atomes de carbone asymťtriques. Vrai.
B. La molťcule A est chirale. Faux.
La molťcule A possŤde un centre de symťtrie.
C. La molťcule B est chirale. Vrai.
Elle possŤde deux atomes de carbone asymťtriques et aucun ťlťment de symťtrie.
D. A et B forment un couple d'ťnantiomŤres. Faux.
E. A et B forment un couple de diastťrťoisomŤres. Vrai.
On rťalise le titrage de la teneur en ion chlorure Cl- d'un volume V0 = 100,0 mL d'une eau minťrale par une solution de nitrate d'argent ( Ag+ +NO3-)
de concentration molaire c = 1,00 mol/L. La rťaction forme du chlorure
d'argent solide. Ce titrage est rťalisť par un suivi conductimťtrique.
On nťgligera l'effet de dilution. De plus on supposera les diffťrentes
conductivitťs molaires ioniques constantes. L'ťvolution de la
conductivitť s en fonction du volume V ajoutť de la solution de nitrate d'argent est donnťe.
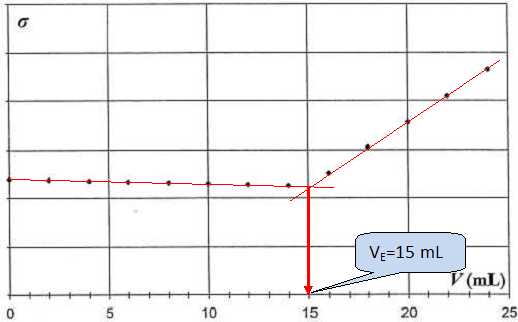
A. Avec certaines rťactions de titrage, la conductivitť peut diminuer aprŤs l'ťquivalence. Faux.
AprŤs l'ťquivalence le rťactif titrant est en excŤs ; on ajoute des ions ŗ la solution et la conductivitť augmente.
B. La conductivitť s'exprime en siemens. Faux.
La conductance s'exprime en siemens, la conductivitť s'exprime en S m-1.
C. La conductivitť d'une solution de chlorure de sodium peu concentrťe est proportionnelle ŗ la concentration en solutť apportť. Vrai.
D.
Le suivi conductimťtrique associť ŗ la courbe proposťe permet
d'affirmer que la conductivitť molaire ionique des ions chlorure est
lťgŤrement supťrieure ŗ celle des ions nitrate. Vrai.
Avant
l'ťquivalence, le nitrate d'argent est en dťfaut. Du point de vue de la
conductivitť, tout revient ŗ remplacer l'ion chlorure par l'ion nitrate
de conductivitť molaire ionique moindre. La conductivitť de la solution
dťcroÓt.
E. La concentration des ions chlorure dans l'eau minťrale vaut 0,15 mol/L. Vrai.
A l'ťquivalence : [Cl-]V0 =VE c ; [Cl-]V0 =VE c / V0 =15*1,00 /100 =0,15 mol/L.
|
|
|