Analyse chimique :
dosage par la méthode de l'étalon interne.
Concours Assistant d'ingénieur Maine
Itrf 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
Culture générale.
L’HPLC est une technique :
A : de cristallisation. Faux.
B : de séparation de molécule. Vrai.
C : de purification. Faux.
En HPLC, phase inverse, quelles ont les phases ?
A : Phase stationnaire apolaire et phase éluante polaire. Vrai.
B : Phase stationnaire polaire et phase éluante apolaire. Vrai.
En HPLC, peut-on utiliser un détecteur de réfractométrie lors
d’une élution en gradient de phase mobile ? Justifier.
Le réfractomètre mesure la variation de l'indice de réfraction
du liquide à la sortie de la colonne. Cet indice dépend de la
température du liquide. On compare cet indice avec celui de la
phase mobile pure, ce dernier sert de référence. Ce détecteur exclut
les variations de composition de la phase mobile. Ce détecteur est
utilisé en mode isocratique.
Que signifie « Colonne C18 »
Les groupes alkyles
greffés sur la phase stationnaire comptent 18 atomes de carbone.
Classer par ordre de polarité croissante les solvants : méthanol,
isopropanol, hexane, eau, dichlorométhane.
Hexane, dichlorométhane,
isopropanol, méthanol, eau.
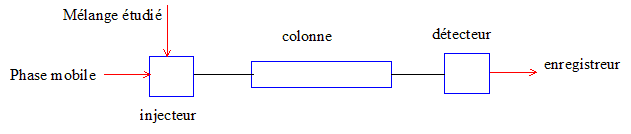
Faire le schéma de principe d’un chromatographe en phase gaz. Présenter
brièvement les différents éléments et leur fonction.
 Entourer dans la liste
suivante les détecteurs de la chromatographie gazeuse :
Entourer dans la liste
suivante les détecteurs de la chromatographie gazeuse :
Conductimètre, réfractomètre, catharomètre ( vrai), spectromètre de
masse ( vrai), ionisation de flamme ( vrai), barette diodes,
fluorimètre, capture d'électrons ( vrai).
Que signifie le sigle RMN ?
Résonance magnétique
nucléaire.
Quelle est la particularité des solvants utilisés en RMN ?
Les solvants sont deutérés
et les molécules
organiques doivent y être solubles.
Ces solvants contiennent en général du TMS (à 0,3 ou 1%), que signifie
ce terme TMS ? A quoi sert-il ?
Le signal des protons du
TMS ( tétraméthylsilane) sert de référence.
Les
12 protons équivalents du TMS présentent une absorption intense à des
champs plus forts que dans la plupart des autres protons. Le pic
correspondant est bien séparé à droite de l'enregistrement.
En
RMN 1H, à quoi ressemble le signal d’un méthyle (CH3)
voisin d’un méthylène (CH2) ?
Le signal de ce méthyle
est un triplet.
|
| .
. |
|
|
Dosage par la
méthode de l’étalon interne.
L’Aspro Accel® est une spécialité appartenant à la
classe des antalgiques et antipyrétiques.
On se
propose de doser l’acide acétylsalicylique et la caféine dans l’Aspro
Accel®.
L’étiquette indique la composition suivante : - acide acétylsalicylique
(aspirine 500 mg)
- caféine (50 mg).
La technique retenue est la chromatographie liquide couplée à un
détecteur UV-visible. Le dosage
est réalisé par étalonnage interne à l’aide de l’acide benzoïque.
L’analyse se fait à la longueur d’onde 270 nm.
L’éluant est composé d’un mélange méthanol 35% et eau 65% avec acide
acétique à 0,5%
Le débit est de 1,2mL/min.
Une solution contenant la caféine, l’acide acétylsalicylique et l’acide
benzoïque à 0,05 mol.L-1 en
chacun des composés a été injectée. Le chromatogramme est le suivant :

|
.
|
|
Identification
des fractions.
On a analysé par RMN 1H la
fraction sortant à 3,07 min.
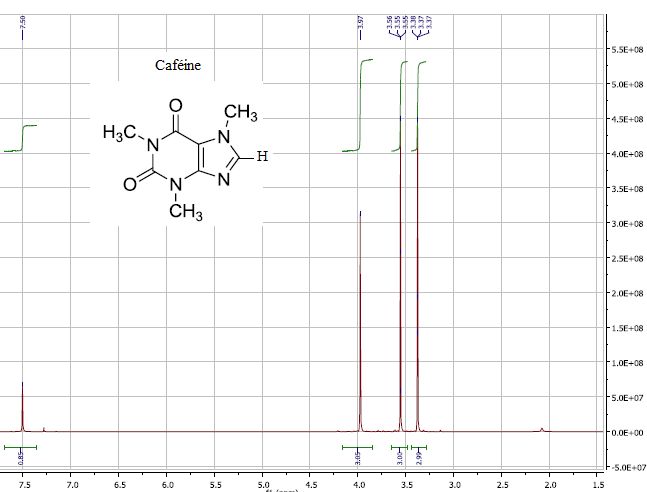
Justifier autant que possible qu’il s’agit
bien de caféine à partir du spectre.
La caféine comporte 4
groupes de protons équivalents, ces derniers n'ont aucun proton proche
voisin : on observera donc des singulets. La courbe d'intégration
indique 3 pour les protons des groupe méthyle et 1 pour le proton du
cycle aromatique.
Le déplacement chimique ( 7,5 ppm) correspond à un proton d'un
cycle aromatique. Les déplacements chimiques vers 3,5 - 4 ppm
correspondent à des groupes méthyles fixés sur un hétéroatome.
De même, on a analysé la fraction sortant à 4,58 min
:
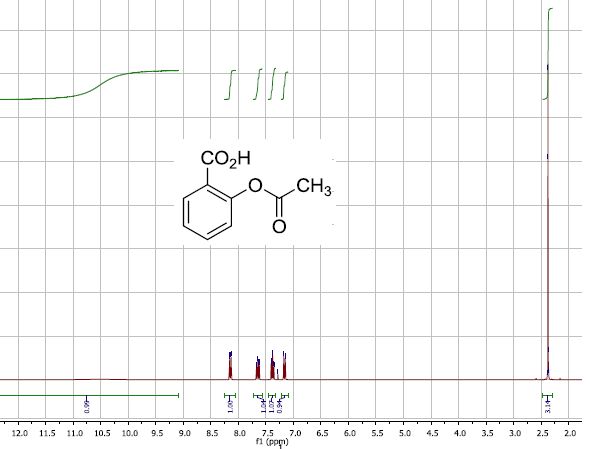
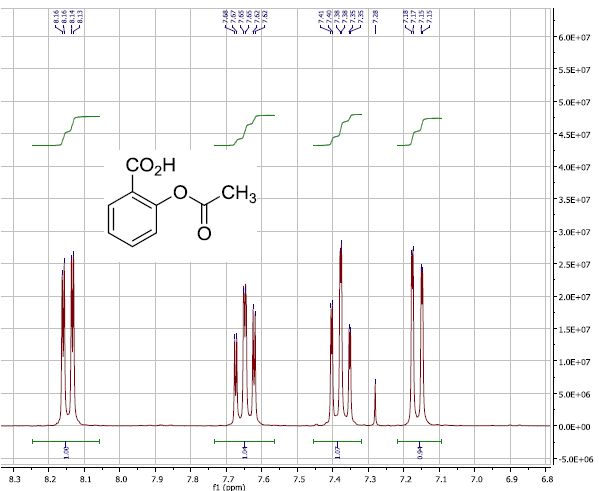
Justifier autant que possible qu’il s’agit bien d’acide
acétylsalicylique à partir des spectres.
Le singulet vers 10,5 ppm
correspond au proton de l'acide carboxylique ; celui vers 2,4 ppm aux 3
protons du groupe méthyle en alpha du groupe ester. Les autres signaux correspondent aux
protons aromatiques.
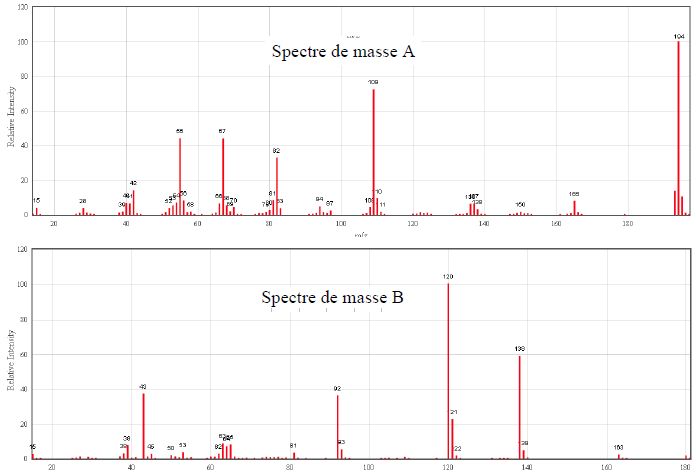
Les deux fractions ont également été analysées par spectrométrie de
masse. Deux enregistrements A et B ont été obtenus en impact
électronique.
Que signifie m/z ? Rapport masse sur
charge pour un ion donné.
Pour chacune des deux molécules, quelle valeur de m/z vous attendez
vous à trouver sur le spectre de masse ?
Lors de l'ionisation par
impact électronique, un électron faiblement lié est éjecté de la
molécule, ce qui conduit à un radical cation ( un électron célibataire
et une charge positive), appelé ion moléculaire ayant même masse que la
molécule initiale. Puis cet ion moléculaire se fragmente.
A : caféine , ion
moléculaire à m/z = 194 ; B : aspirine, ion moléculaire à m/z = 180.
Sur le spectre de masse A, quel est le pic majoritaire ? Quel est le
pic pseudo-moléculaire ?
Le pic majoritaire
correspond à m/z = 194 ( pic moléculaire). Le pic pseudo-moléculaire correspond soit
à l'ajout d'un proton (M+H)+ : masse M+1, charge 1, soit à la perte
d'un proton ( M-H)+ : masse M-1, charge -1.
Sur le spectre de masse B, quel est le pic majoritaire ? Comment s’est
formé l’ion m/z 43 ? Quelle est sa formule ?
Quelle indication vous donne-t-il sur l’identité de la molécule
correspondant à ce spectre ?
Le pic majoritaire est
situé à m/z = 120. L'ion à
m/z = 43 correspond à CH3-CO+, coupure de la liaison C-O du groupe ester.
|
|
Dosage du
comprimé
Afin de déterminer le facteur de réponse des 2
molécules par rapport à l’étalon interne, une solution avec les 3
composés, dont les masses sont indiquées dans le tableau, est injectée.
Composé
|
Masse
de composé (g)
|
%
massique
|
Aire
|
%
Aire
|
Caféine
|
0,024
|
17,52
|
44725
|
61,65
|
Aspirine
|
0,055
|
40,15
|
10447
|
14,40
|
Acide
benzoïque
|
0,058
|
42,33
|
17367
|
23,94
|
Calculez le facteur de réponse pour les 2
molécules par rapport à l’étalon interne.
Kcaféine =%mcaféine / %mac.benzoîque
* %Aac benzoïque / %Acaféine=17,52 /
42,33 *23,94 / 61,65 =0,161.
Kaspirine =%maspirine / %mac.benzoîque
* %Aac benzoïque / %Aaspirine=40,15 /
42,33 *23,94 / 14,4 =1,577.
On réalise ensuite la manipulation suivante sur le comprimé :
Extraction des principes actifs de l’Aspro Accel® : dissoudre un
comprimé dans un becher de 100 mL avec un peu d’eau ultra-pure.
Compléter à 100 mL avec une fiole jaugée. Filtrer la solution sur
papier filtre. Dégazer 10 minutes à la cuve à ultra-sons. Prélever 5 mL
de la solution, ajouter 0,005 g d’acide benzoïque et compléter avec du
méthanol au trait de jauge. Injecter.
Les résultats de l’analyse de l’échantillon sont donnés ci-dessous : A cafeine
=53320, Aaspirine =52354, Aac benzoïque = 16089.
%A cafeine =43,79, %Aaspirine =43,00, %Aac benzoïque = 13,21.
Déterminer la concentration en acide acétylsalicylique et en caféine
dans l’échantillon, puis dans un comprimé d’Aspro Accel®.
Dm=%Aac
benzoïque +Kcaféine %A cafeine +Kaspirine %Aaspirine =13,21 +0,161*43,79 +1,577*43,0 =88,07.
%mcaféine =Kcaféine %A cafeine / Dm=0,161*43,79
/ 88,07 =0,0800 ou 8,00%.
%maspirine =Kaspirine %Aaspirine / Dm= 1,577*43,00 / 88,07
=0,770 ou 77,0 %.
%mac benzoïque =15 % ; masse de
l'échantillon : m = 0,005 / 0,15 =0,0333g = 33,3 mg.
Masse d'aspirine dans l'échantillon : 33,3 *0,77 =25,66 ~25,7 mg ;
masse de caféine dans l'échantillon : 33,3 *0,080 =2,666 ~2,67 mg.
Masse d'aspirine dans le comprimé : 25,7 *100 / 5 =514 mg ; masse de
caféine dans le comprimé : 2,67*100/5 =53,3 mg.
|
|
|