QCM : chimie
organique.
Concours kinť EFOM 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
|
|
|
|
|
|
|
1. Une solution d'ion cťrium (IV)
est prťparťe par dissolution de 9,96 g de sulfate de cťrium (IV) Ce(SO4)2
(s) dans 100 mL d'eau distillťe. L'ion cťrium (IV) est un oxydant. M(Ce(SO4)2
) =
332 g/mol.
- Le titre massique en sulfate de cťrium (IV) apportť est de l'ordre de
1 102 g/L.Vrai.
9,96 g dissout dans 0,1 L
ou 99,6 g dissout dans 1 L.
- La concentration molaire effective de
l'ion sulfate est ťgale ŗ 0,600 mol/L.Vrai.
n=m/M
=9,96 / 332 =0,0300 mol.
C = n/V = 0,0300 /0,100 =
0,300mol ; [sulfate] = 2 C = 0,600 mol/L.
- La solution contient plus d'anions que de cations. Vrai.
La
solution est ťlectriquement neutre : 4 [Ce4+] = 2 [SO42-]. 2[Ce4+]
= [SO42-].
- Le caractŤre oxydant de l'ion cťrium
(IV) tient ŗ sa capacitť ŗ cťder un ou plusieurs ťlectrons. Faux.
Un oxydant est
susceptible de gagner un ou plusieurs ťlectrons.
2.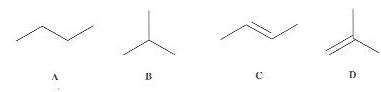
- Toutes ces molťcules sont des
hydrocarbures.Vrai.
- A et B
sont des isotopes. Faux.
A et B sont des isomŤres.
- A pression fixťe, la molťcule A possŤde la mÍme tempťrature
d'ťbullition que la molťcule B. Faux.
- Les molťcules C et D prťsentent la stťrťoisomťrie Z / E. Faux.
3. L'eu-mťlanine et
la phťo-mťlanine sont responsables de la couleur des cheveux. Ce sont
des pigments naturels obtenus par polymťrisation. Ces deux molťcules
dťrivent par oxydations successives, de la tyrosine qui a pour formule :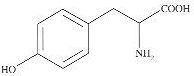
- Cette formule de la molťcule de tyrosine est une ťcriture
topologique. Faux.
Sur une formule topologique, on n'ťcrit pas les atomes de carbone.
- La formule brute de la tyrosine est C9H11NO3. Vrai.
- La tyrosine possŤde, entre autre, un groupe carboxyle. Vrai.
- La tyrosine possŤde un seul atome de carbone asymťtrique. Vrai.
Le carbone porteur du
groupe amino et du groupe carboxyle.
4. L'acide
tartrique est le nom usuel d'une molťcule de formule brute C4H6O6.
Il se forme notamment dans la fermentation du jus de raisin qui conduit
au vin. On donne une reprťsentation spatiale de cette molťcule.
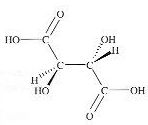
- L'acide tartrique possŤde 4 groupes hydroxyle et deux groupes
carboxyle. Faux.
L'acide
tartrique possŤde deux
groupes hydroxyle et deux grroupes carboxyle.
- L'acide
tartrique possŤde un seul atome de carbone asymťtrique. Faux.
L'acide tartrique possŤde deux atomes de
carbone asymťtrique.
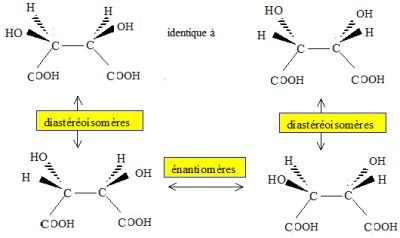
- La molťcule reprťsentťe n'est pas chirale. Vrai.
Elle possŤde un centre de
symťtrie.
-L'acide tartrique possŤde 4 couples de diastťrťoisomŤres. Faux.
|
| .
. |
|
|
5.
Le propane est un hydrocarbure gazeux dans les conditions normales de
tempťrature et de pression. Sa combustion complŤte dans le dioxygŤne de l'air produit du
dioxyde de carbone et de l'eau. Vm = 24 L / mol.
- La formule du propane est C3H6. Faux.
C3H8.
- La masse molaire du propane est 42
g/mol.
Faux.
44 g/mol.
- La combustion complŤte de 48 L de propane libŤre 6,0 moles de dioxyde
de carbone. Vrai.
C3H8 +5
O2 ---> 3 CO2
+ 4H2O.
n(mťthane) = 48 / 24 = 2
moles ; n( CO2) = 3 n(mťthane) = 6,0 moles.
- Le spectre RMN 1H du propane comporte un unique triplet
et un unique quadruplet. Vrai.
|
.
|