QCM chimie.
Concours kinť ader.. 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
|
|
|
|
|
|
|
|
|
64. D'aprŤs concours manipulateur radio ST Germain 2010.
Dans un ballon, on rťalise la rťaction entre le carbonate de calcium et l'acide chlorhydrique ( H3O+aq+ Cl-aq ). Le dioxyde de carbone formť est recueilli par dťplacement d'eau dans une ťprouvette graduťe.
Un ťlŤve verse dans le ballon un volume VS =100 mL d'acide
chlorhydrique ŗ 0,100 mol/L. A la date t=0, il introduit rapidement
dans le ballon 2,00 g de carbonate de calcium tandis qu'un camarade
dťclenche un chronomŤtre. Les ťlŤves relŤvent le volume VCO2
de dioxyde de carbone dťgagť en fonction du temps. Puis aprŤs avoir
calculť les valeurs de l'avancement, ils ont reportťs les rťsultats sur
le graphe x = f(t). On donne Vm = 24 L/mol.
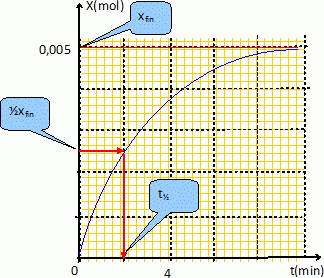
La rťaction chimique ťtudiťe peut Ítre modťlisťe par l'ťquation :
CaCO3(s) + 2 H3O+aq = Ca2+aq + CO2(g) + 3 H2O(l).
Dťterminons les quantitťs de matiŤre initiales de chacun des rťactifs.
n(H3O+aq) = 0,1 VS = 0,1*0,1 = 0,01 mol.
M(CaCO3) = 40 +12+3*16 = 100 g/mol ; n(CaCO3) = m / M = 2,0 / 100 = 0,02 mol.
0,01 mol d'acide rťagit avec 0,005 mol de carbonate de calcium. Ce dernier est en excŤs.
Il se forme 0,005 mol de dioxyde de carbone soit 0,005*24 = 0,12 L.
Les
rťponses exactes sont A et B.
65. CaCl2 anhydre.
CaCl2(s) ---> Ca2+ aq +Cl-aq.
Quantitť de matiŤre initiale de chlorure de calcium.
M(CaCl2) =40 +2*35,5 = 111 g/mol.
n(CaCl2) = 1,11 103 / 111 = 10,0 mol.
La dissolution du solide ťtant totale, l'avancement final est ťgal ŗ 10,0 mol.
Concentration finale des ions calcium : [Ca2+aq] = n(CaCl2) / V = 10,0 / 2,0 = 5,0 mol/L.
La solution est ťlectriquement neutre : [Cl-aq]=2[Ca2+aq] = 10 mol/L
Les
rťponses exactes sont A, C et E.
A est vrai si on ne tient pas compte des chiffres significatifs, sinon faux.
|
|
|
|
66. Chaufferette chimique.D'aprŤs bac S mťtropole 09 /2011.
Une chaufferette chimique contient une solution aqueuse S0 d'ťthanoate de sodium (CH3COO-aq + Na+aq).
Le volume de la solution est V0 = 100 mL et sa masse est m =130 g.
La solution S0 ťtant trop concentrťe pour Ítre dosťe directement, on prťpare une solution S1 en diluant 100 fois S0.
Titrage de la solution S1.
On place dans un becher un volume V1 = 25,0 mL de S1.
On rťalise un titrage par pHmťtrie par une solution d'acide chlorhydrique ( H3O+aq+Cl-aq) de concentration cA = 0,20 mol/L. On note VA le volume de la solution d'acide chlorhydrique versť.
L'ťquation de la rťaction chimique support du dosage s'ťcrit :
H3O+aq + CH3COO-aq = CH3COOH aq +H2O(l).
A l'ťquivalence, les
quantitťs de matiŤre des rťactifs mis en prťsence sont en proportions
stoechiomťtriques. Avant l'ťquivalence, l'un des rťactifs est en excŤs,
aprŤs l'ťquivalence, l'autre rťactif est en excŤs.
n(H3O+aq) = CAVA eq ; n(CH3COO-aq) =V1 [CH3COO-aq]1.
CAVA eq = V1 [CH3COO-aq]1 avec VA eq =9,0 mL.
Concentration c1 en ion ťthanoate dans la solution S1.
[CH3COO-aq]1 = CAVA eq =/ V1 =0,20*9,0 /25=0,0704 ~0,072 mol/L.
Par suite c0 = 100 c1 = 100 *0,072 = 7,2 mol/L ou 0,72 mol dans 100 mL.
La solubilitť de l'ťthanoate de sodium ťtant de 4,5 mol/L ŗ 25įC, la solution est saturťe.
M(ťthanoate de sodium )~ 100 g/mol.
Masse d'ťthanoate de sodium dans la chaufferette : 0,72*100 ~72 g.
Les
rťponses exactes sont C et D.
67. RMN.
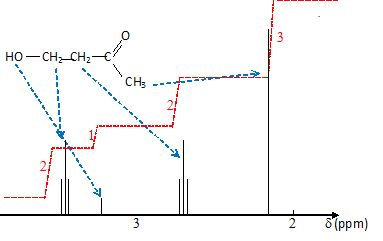
La
rťponse exacte est D.
68. Combustion d'un hydrocarbure.
CxHy + (x+0,25y)O2 ---> xCO2 +ĹyH2O.
M(CxHy) =12 x+y.
Quantitť de matiŤre de dioxyde de carbone n (CO2)=4,4 / M(CO2) = 4,4 /44 = 0,10 mol.
Quantitť de matiŤre d'eau : n(H2O) = 1,8 /M(eau) = 1,8 / 18 = 0,10 mol.
Par suite x = Ĺy soit y = 2x. L'hydrocarbure est un alcŤne de formule brute CxH2x.
Masse de carbone dans l'hydrocarbure : 4,4 /44 *12 =1,2 g.
Masse d'ťlťment hydrogŤne dans l'hydrocarbure : 1,8 /18*2 = 0,2 g.
masse m d'hydrocarbure : 1,4 g.
Les
rťponses exactes sont D et E.
|
69. pH d'une solution.
Quantitťs
de matiŤre initiales : n( ac. sulfamique) =10 / M(ac. sulfamique)
~ 10 / 100 =0,10 mol dans 500 mL d'eau soit 0,10 *25 / 500 =0,005 mol
dans 25 mL.
n(soude) = cV =0,25 *0,020 = 0,005 mol.
Les quantitť de matiŤre des rťactifs sont en proportions
stoechiomťtriques. La soude est une base forte, l'acide sulfamique est
un acide fort.
Le pH du mťlange est ťgal ŗ 7. Rťponse C.
70. Rendement d'une synthŤse.
2 benzaldťhyde + propanone ---> produit +2H2O.
Quantitťs de matiŤre initiales : n(benzaldehyde) = 5,3 / 106 = 0,050 mol.
n(propanone) ~ 3,0*0,80 / 60 ~0,04 mol ( en excŤs ).
0,050 mol de benzaldehyde rťagit avec 0,025 mol de propanaone pour donner 0,025 mol de produit.
On peut espťrer obtenir au mieux 0,025 M(produit) = 0,025*234 = 5,85 g de produit.
Rendement : masse rťelle / masse expťrimentale *100 = 4,68 / 5,85 *100 ~80 %. Rťponse A. |
|