Autour du
salicylate de méthyle, Bac S Antilles 2018
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
.
.
|
|
1. Synthèse du salicylate de méthyle à partir de l'acide salicylique et du méthanol
1.1. Ecrire la formule semi-développée du méthanol, mettre en évidence le groupe caractéristique et nommer la fonction associée.
H3C-OH ; groupe hydroxyle ; fonction alcool primaire..
1.2 L'acide salicylique réagit avec le méthanol pour former du salicylate de méthyle et un produit nomé A.
1.2.1. Ecrire l'équation de la réaction et identifier A. A quelle catégorie appartient cette réaction ?
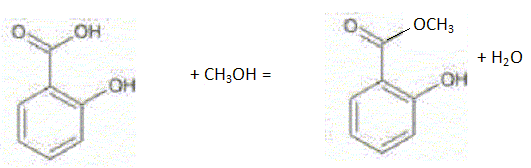 Réaction d'estérification, limitée par l'hydrolyse de l'ester.
Réaction d'estérification, limitée par l'hydrolyse de l'ester.
On substitue à l'hydrogène de la fonction acide carboxylique, le groupe méthyle CH3.
1.3. Une synthèse est réalisée en laboratoire en introduisant 10,0 g d'acide salicylique et 10,0 mL de méthanol.
1.3.1. Déterminer les quantités de matière des réactifs.
acide salicylique n1 = 10,0 / M(acide salicylique ) = 10,0 / 138 = 7,25 10-2 mol.
méthanol : n2 = 10,0 r / M(méthanol) = 10,0 x0,792 / 32 =0,2475 ~0,248 mol.
1.3.2. En déduire le réactif limitant.
Le méthanol est en large excès ; l'acide salicylique est le réactif limitant.
1.3.3. La masse de salicylate de méthyle obtenue est de 6,3 g. Déterminer le rendement de cette synthèse.
On peut espérer obtenir au mieux ( si réaction totale) 7,25 10-2 mol de salicylate de méthyle.
Soit 7,25 10-2 M(ester) = 7,25 10-2 x152 = 11,014 g.
Rendement = masse expérimentale / masse théorique = 6,3 / 11,014 ~0,57 ( 57 %).
|
|
...
|
|
2. Pommades contre les douleurs musculaires.
Pour pénétrer la surface de la peau, les principes actifs ne doivent pas être chargés. Le pH de la peau est proche de 5.
Acide salicylique / ion salicylate : pKA1 = 3.
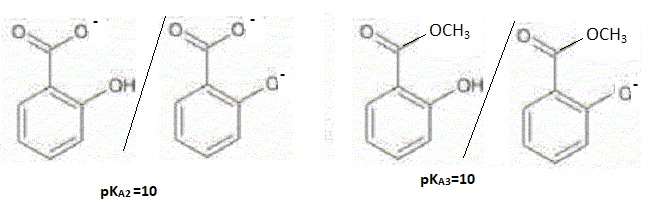
Entre
le salicylate de méthyle et l'acide salicylique lequel est préféré pour
un usage dans les pommades contre les douleurs musculaires ? Justifier.
Les principes actifs pénétrant la peau ( pH = 5) ne doivent pas être chargés.
log ( [A- ] / [AH] )= pH- pKa.
Couple acide salicylique / ion salicylate : log ( [A- ] / [AH] )= 5-3 = 2 ; log ( [A- ] / [AH] )= 102.
La forme ionique représente environ 99 % du produit.
Couple salicylate de méthyle / ion correspondant : log ( [A- ] / [AH] )= 5-10 = -5 ; log ( [A- ] / [AH] )= 10-5.
La forme acide, non ionique représente pratiquement 100% du produit.
Le salicylate de méthyle est retenu.
|
|
.
|
|