L'arôme
de vanille,
bac Métropole 2022.
Chromatographie, titrage acide base
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
.
.
|
..
..
......
...
|
1. Étude de produits commerciaux "vanillés".
On souhaite étudier trois produits du commerce "vanillés" :
- produit 1 : produit commercial, liquide, obtenu par macération de gousses de vanille dans un
mélange eau / éthanol ;
- produit 2 : sucre vanillé ;
- produit 3 : sucre vanilliné.
Q1. Indiquer si les molécules de vanilline et d’éthylvanilline sont des isomères de constitution. Justifier.
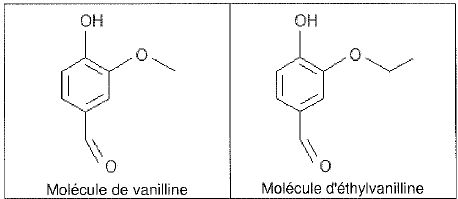
Non, elles ne possèdent pas la même formule brute.
Q2. Représenter la formule topologique de la molécule de vanilline.
Q3. Sur la molécule représentée à la question Q2, entourer deux groupes caractéristiques présents et
nommer pour chacun d’eux la famille fonctionnelle associée.
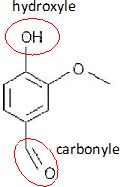
Familles associées : alcool et aldehyde.
On extrait la vanilline potentiellement présente du produit 2 puis du produit 3 selon le protocole ci-dessous :
- introduire, dans un erlenmeyer, 30 mL d’eau distillée et 1,0 g de produit « vanillé » ;
- introduire la solution aqueuse dans une ampoule à décanter et y ajouter 10 mL d’acétate d’éthyle
ainsi qu’une spatule de chlorure de sodium ;
- agiter l’ensemble et dégazer régulièrement ;
- laisser décanter le mélange puis récupérer la phase organique.
Q4. Schématiser l’ampoule à décanter après agitation dans le cas du produit 2 en précisant la position
relative des phases et en indiquant celle qui contient la vanilline. Justifier.
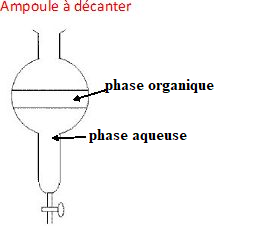
Densité de l'acétate d'éthyle : 0,897.La phase la plus dense occupe la position inférieure.
La vanilline est très souble dans l'acétate d'éthyle, très peu soluble dans l'eau salée.
Pour vérifier la présence ou non de vanilline dans les trois produits du commerce, on réalise une
chromatographie sur couche mince.
Après révélation sous lampe UV, on obtient le chromatogramme suivant.
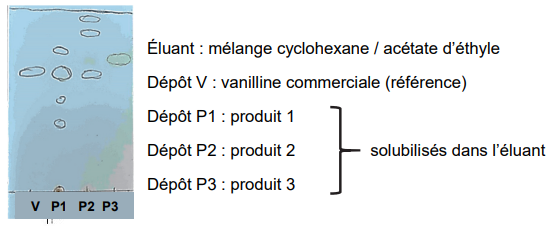
Q5. Identifier, en justifiant, les produits du commerce contenant de la vanilline.
P1 et P2 présentent une tache avec le même rapport frontal que la vanilline de référence.
2. Titrage de la vanilline contenu dans le produit 1
On s’intéresse dans cette partie au produit commercial obtenu par macération de gousses de vanille. La
législation impose, pour obtenir l’appellation « extrait de vanille », une masse minimale de 2 g de vanilline
par kilogramme d’extrait. Dans certains produits commercialisés, cette masse peut atteindre plusieurs
dizaines de grammes.
Pour vérifier si le produit 1 répond à cette condition, on se propose de déterminer la masse de vanilline
contenue dans un échantillon du produit commercial par un titrage suivi par pH-métrie.
On introduit 0,31 g de produit 1 dans une fiole jaugée de 100,0 mL que l’on complète jusqu’au trait de jauge
avec une solution aqueuse d’hydroxyde de sodium. On note S la solution obtenue. On réalise le titrage
d’une prise d’essai de 50,0 mL de solution S par une solution aqueuse d’acide chlorhydrique de
concentration égale à CA=4,1×10–3 mol·L–1. La courbe du titrage est donnée.
Q6. Justifier que la vanilline se trouve sous forme d’ion vanillinate, noté A–, au début du titrage.
La courbe de la figure 4 est composée de deux sauts de pH :
- un premier saut qui correspond au titrage des io
pKA du couple vanilline / ion vanillinate noté AH / A– à 25 °C : pKA = 7,4 ;
pH initial = 10. A pH supérieur à pKa, la forme base conjuguée A- prédomine.
La courbe est composée de deux sauts de pH :
- un premier saut qui correspond au titrage des ions hydroxyde présents en excès ;
- un deuxième saut qui correspond au titrage de l’ion vanillinate.
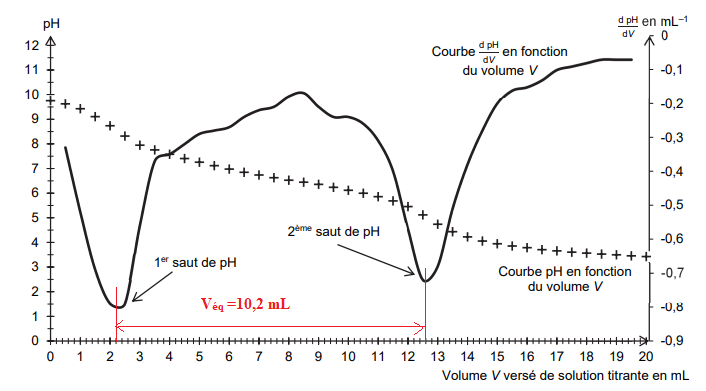
On admet que le volume d’acide chlorhydrique nécessaire pour titrer l’ion vanillinate est égal à la différence
des deux volumes entre les deux équivalences observées.
Q7. Écrire l’équation de la réaction support du titrage entre l’ion vanillinate et l’acide chlorhydrique.
A-aq + H3O+aq --> AH aq + H2O(l)
Q8. Vérifier si l’appellation "extrait de vanille" peut être attribuée à l’extrait étudié.
n(A-) =Véq CA=10,2 x4,1×10–3 =4,08 10-2 mmol
M (AH) = 152 g / mol.
masse de vanilline : 4,08 10-2 x 152 =6,2 mg dans 50 mL soit 12,4 mg = 0,0124 g dans 100 mL ou dans 0,31 g de produit 1.
0,0124 / 0,31 x1000 =40 g de vanilline par kg d'extrait.
" masse minimale de 2 g de vanilline
par kilogramme d’extrait ".
L’appellation "extrait de vanille" peut être attribuée à l’extrait étudié.
|
|