Besoins en
magnťsium, bac G
Amťrique du Sud 2022.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts.
.
| . |
.
.
|
|
.
..
|
..
..
......
...
|
Le
magnťsium est un oligoťlťment indispensable ŗ notre organisme. Les
cartouches ę Edition Mg2+ Ľ disponibles pour des carafes filtrantes
permettraient de faire consommer une eau enrichie en magnťsium.
Dans une cartouche filtrante ę Edition Mg2+ Ľ, l’eau passe notamment
par une rťsine ťchangeuse d'ions qui va ťliminer le tartre et les
mťtaux lourds ; les ions calcium prťsents dans l’eau sont alors
remplacťs par des ions magnťsium […] D’aprŤs https://www.bwt.com/fr-fr/.
Le but de cet exercice est de vťrifier l’efficacitť de ces cartouches
filtrantes relative au remplacement des ions calcium par des ions
magnťsium.
Donnťes - Masses molaires : M(Mg) = 24,3 g∑mol-1 ; M(Ca) =
40,1 g∑mol-1
- Mťthode de dťtermination de la concentration totale en ions magnťsium
et calcium. La concentration totale en ions magnťsium et en ions
calcium d’une eau peut Ítre dťterminťe gr‚ce ŗ un titrage par l’EDTA
(acide ťthylŤne diamine tťtraacťtique) en prťsence d’un indicateur
colorť de fin de rťaction et d’une solution tampon permettant de
maintenir le pH de la solution entre 9 et 10.
La concentration de la solution d’EDTA utilisťe est C=1,0◊10−2
mol⋅L−1. En milieu basique, l’EDTA contient des ions Y4−
(ions ťthylŤne diamine tťtraacťtate) qui rťagissent avec les ions
magnťsium (Mg2+) et avec les ions calcium (Ca2+).
Ces transformations chimiques sont modťlisables par deux rťactions
reprťsentťes par les ťquations suivantes :
Mg2+(aq) + Y4−(aq) → MgY2−(aq) ;
Ca2+(aq) + Y4−(aq) → CaY2−(aq)
- Mťthode de dťtermination de la concentration en ions calcium.
La concentration en ions calcium d’une eau est dťterminťe gr‚ce ŗ un
titrage par l’EDTA, ŗ un pH supťrieur ŗ 12, en prťsence d’un indicateur
colorť de fin de rťaction. Dans ce domaine de pH, les ions magnťsium
forment un prťcipitť. La concentration de la solution d’EDTA utilisťe
est C=1,0◊10−2 mol⋅L−1. La rťaction, support du
titrage, modťlisant la transformation s’ťcrit : Ca2+(aq) + Y4−(aq)
→ CaY2−(aq).
Sur
de l’eau obtenue aprŤs filtration avec une carafe munie de la cartouche
ę ťdition Mg2+ Ľ, on rťalise les deux titrages dťcrits pour dťterminer
les concentrations des ions magnťsium et calcium d’une part et les ions
calcium seuls d’autre part. Les deux titrages sont rťalisťs sur un
volume V=100,0 mL d’eau filtrťe. Les rťsultats obtenus sont les
suivants :
| Volumes d’EDTA versťs |
Eau filtrťe |
| Volume VE (en mL)
d’EDTA versť pour atteindre l’ťquivalence lors du titrage des ions
calcium |
8,8
|
| Volume VE (en mL)
d’EDTA versť pour atteindre l’ťquivalence lors du titrage des ions
magnťsium et des ions calcium |
10,8
|
1. Rťaliser le schťma lťgendť du
montage permettant de rťaliser le titrage des ions calcium prťsents
dans une eau.
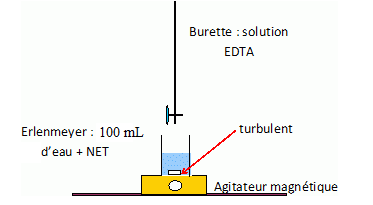
2. Pourquoi le
titrage des ions calcium seuls est-il rťalisť ŗ un pH supťrieur ŗ 12 ?
A pH supťrieur ŗ 12, seuls les ions magnťsium forment un prťcipitť.
3. Dťterminer la
concentration en quantitť de matiŤre en ions calcium de l’eau filtrťe.
A l'ťquivalence : CVE = V [Ca2+] ; [Ca2+] = CVE / V =1,0 10-2
x 8,8 / 100 =8,8 10-4 mol / L = 0,88 mmol / L.
4. Montrer que la concentration en
quantitť de matiŤre en ions magnťsium est ťgale ŗ 0,20 mmol∑L−1.
A l'ťquivalence : CVE
= V ([Ca2+] +[Mg2+] ) ; [Ca2+] +[Mg2+] = CVE / V =1,0 10-2
x 10,8 / 100 =10,8 10-4 mol / L = 1,08 mmol / L.
[Mg2+] =1,08
-0,88 =0,20
mmol∑L−1.
Un
technicien de laboratoire procŤde ŗ l’analyse de l’eau du robinet non
filtrťe et fournit les rťsultats suivants :
| Concentrations en quantitť
de matiŤre |
Eau non filtrťe |
| Concentration en quantitť de
matiŤre des ions calcium |
2,2
mmol / L
|
| Concentration en quantitť de
matiŤre des ions calcium et magnťsium |
2,3
mmol / L
|
5.
Les rťsultats obtenus sont-ils en accord avec les propriťtťs annoncťes
pour la carafe filtrante munie de la cartouche ę Edition Mg2+ Ľ ?
[Mg2+] =2,3 -2,2 =0,10 mmol∑L−1.
Seul
2,2 -0,88 =1,32 mmol / L d' ion calcium prťsents dans l’eau sont alors
remplacťs par des ions magnťsium.
L'efficacitť de cette cartouche reste donc insuffisante.
6. Un adulte de masse 70 kg peut-il
couvrir ses besoins journaliers en magnťsium en consommant uniquement
de l’eau filtrťe ?
En France, pour un adulte, l’Agence Nationale de Sťcuritť Sanitaire de
l’Alimentation, de l’Environnement et du Travail (ANSES) a conseillť un
apport en magnťsium de 6 mg / jour / kg.
6 x 70 = 420 mg =0,42 g de magnťsium par jour.
0,42 / M(Mg) = 0,42 / 24,3 =0,017 mol = 17 mmol.
L'eau filtrťe apporte 0,20 mmol∑L−1d'ion
magnťsium.
Il faudrait donc boire 17 / 0,2 ~85 L d'eau filtrťe.
Un adulte de masse 70 kg ne
peut pas couvrir ses besoins journaliers en magnťsium en consommant
uniquement de l’eau filtrťe.
|