Une boîte cubique d’arrête a contient 𝑛 = 10
3
moles d’argon (masse molaire M=40 g. mol
-1). Dans ce problème, on note
𝑥, 𝑦 et 𝑧 les coordonnées cartésiennes ; O est
l’origine du repère
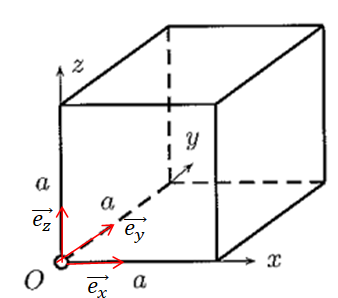 13.
13. Calculer le nombre N d’atomes dans la boîte et la masse m d’un atome d’argon. On rappelle la valeur approximative de
la constante d’Avogadro 𝑁
A ≈ 6.10
23 mol
-1
.
A) 𝑁 ≈ 6.10
23 et 𝑚 ≈ 6,7.10
-23 kg.
B) 𝑁 ≈ 6.10
23 et 𝑚 ≈ 6,7.10
-26 kg.
C) 𝑁 ≈ 6.10
26 et 𝑚 ≈ 6,7.10
-23 kg.
D) 𝑁 ≈ 6.10
26 et 𝑚 ≈ 6,7.10
-26 kg.
Vrai.
m = 0,040 / (6 10
23) ~ 6,7.10
-26 kg.
N = 10
3 x 6 10
23 =6 10
26.
14. Un des atomes vient heurter la paroi en x=a, avec un vecteur vitesse
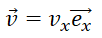
. La paroi étant parfaitement rigide,
l’atome rebondit et repart dans la direction incidente avec le vecteur vitesse
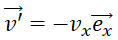
. Déterminer la variation du
vecteur quantité de mouvement de l’atome.
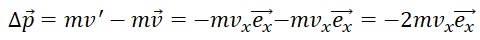
Réponse
C.
15. On admet que l’atome possède un mouvement rectiligne et uniforme, le long de l’axe (𝑂𝑥), jusqu’à ce qu’il heurte de
nouveau la paroi. On admet aussi que lors d’une collision, l’atome, qui arrive avec un vecteur vitesse orthogonal à une
paroi, rebondit avec un vecteur vitesse opposé au vecteur vitesse incident (avant le choc), sans changer sa norme.
Calculer la durée
t qui sépare deux chocs successifs sur la paroi située en x=a et en déduire N
c
qui désigne le nombre
de chocs par seconde de cet atome avec cette paroi.
A) t = 2a / v et N
c = 2 s
-1.
B) t = 2a / v et N
c = v / (2a).
Vrai.
C) t = a / v et N
c = v / a.
D) t = a / v et N
c = 1 s
-1.
L'atome parcourt la distance 2a à la vitesse v :
t = 2a / v.
N
c =1 /
t = v / (2a).
16. On admet que la paroi reçoit à chaque collision la quantité de mouvement
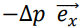
. Quelle est la force subie par la
paroi située en x=a en raison des chocs répétés de l’atome ?
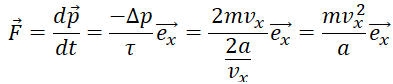
Réponse
A.
17. En réalité, comme les atomes de la boîte n’ont pas tous le même vecteur vitesse, on doit remplacer, dans l’expression
précédente, v
2x par v
2m
/ 3 où v
2m
est la moyenne sur tous les atomes du carré de la norme des vecteurs vitesse de chaque
atome. Donner la ou les expressions correctes de la pression P exercée par le gaz d’atomes sur la paroi située en x=a ;
on note n
v
le nombre d’atomes par unité de volume dans la boîte.
Surface de la paroi S = a2 ; volume de la boîte V = a3.
Pression = force / surface = N F / S = N m v
2m / (3a3).
nv = N / a3 ; P = nv m v
2m / 3 .
Réponses
B et
C.
18. En admettant que le gaz dans la boîte est un gaz parfait et que la pression ci-dessus est celle qui intervient dans la loi
des gaz parfaits, donner l’expression de la température 𝑇 de ce gaz.
T = PV / nR =
nv m v
2m a3/ (3nR).
nv a3 = N ; n= N / NA= nv a3 / NA.
T =mNA v
2m / (3R) = M v
2m / (3R).
Réponse
A.