La piqûre acétique est un phénomène qui intervient lorsque l’éthanol d’un vin se transforme en acide
éthanoïque suite à une exposition prolongée à l’air et notamment au dioxygène. On étudie, dans cet
exercice, l’acide éthanoïque (CH
3COOH) formé dans le vin.
Au laboratoire, il est possible de déterminer la concentration en masse d’acide éthanoïque contenu
dans le vin en réalisant un titrage pH-métrique. Pour cela, il faut d’abord réaliser une distillation et
ensuite titrer le distillat obtenu.
Dans un ballon de 200 mL, on introduit :
- 20,0 mL de vin décarboniqué ;
- 35 mL d’eau distillée ;
- une pointe de spatule d’acide tartrique.
On distille en utilisant une colonne de Vigreux et on recueille avec soin le distillat que l’on
transvase dans un bécher.
On titre l’acidité du distillat avec une solution aqueuse d’hydroxyde de sodium à la concentration
en quantité de matière C
B= 0,150 mol / L
.
Ceci permet de recueillir 80 % de l’acide éthanoïque du vin.
.
1. Lister, en justifiant, les équipements de protection individuelle à utiliser pour mettre en œuvre
ce dosage au laboratoire.
l'acide tartrique et l'hydroxyde de sodium sont corrosifs. Port de blouse, gants et lunette de protection.
2. Choisir, en justifiant, le montage expérimental à utiliser pour la distillation parmi les trois
propositions suivantes :
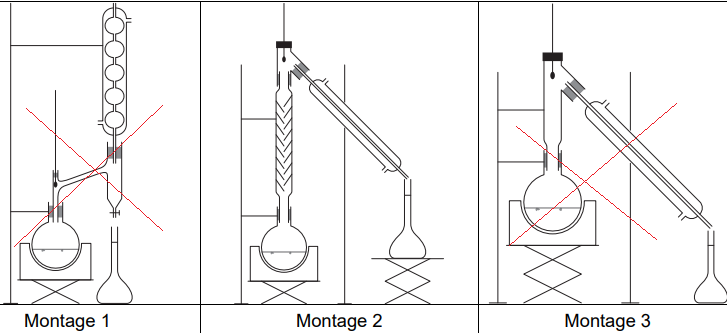 3.
3. Écrire l’équation de la réaction de titrage qui s’effectue entre l’acide éthanoïque (CH
3COOH) et
les ions hydroxyde (HO
–
).
CH
3COOH aq + HO
-aq --> CH
3COO
-aq + H
2O(l).
On considère qu’une réaction chimique peut être support d’un titrage lorsque sa constante
d’équilibre est supérieure à 10
4.
4. Déterminer la constante d’équilibre K associée à la réaction de titrage à l’aide de Ka et Ke, puis
conclure.
K
a =[ CH
3–COO
–
(aq)] [ H
3O
+aq] / [CH3
–COOH(aq)] ; Ke = [ H
3O
+aq] [ HO
-aq]
K = [ CH
3–COO
–
(aq)] / ( [CH
3–COOH(aq)] [ HO
-aq]) .
K = [ CH
3–COO
–
(aq)]
[ H3O+aq]/ ( [CH
3–COOH(aq)] [ HO
-aq]
[ H3O+aq]) = K
a
/Ke = 10
-4,2 / 10
-14 =6,3 10
9.
Cette valeur étant supérieure à 10
4, la réaction est totale et peut être utilisée pour un titrage.
5. Déterminer graphiquement la
valeur du volume versé à l’équivalence Ve.
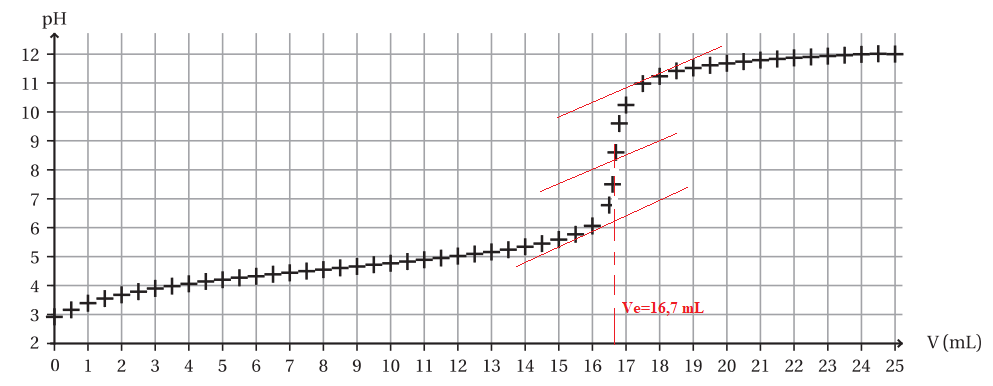 6.
6. Calculer la valeur de la quantité de matière de l’acide éthanoïque présente dans l’échantillon de
vin titré.
n = C
B Ve =0,150 x 16,7 =2,505 ~2,51 mmol.
7. Montrer que la valeur de la concentration en quantité de matière de l’acide éthanoïque contenu
dans l’échantillon de 20,0 mL est de 0,126 mol / L.
2,51 / 20,0 =0,125 mol / L.
.
8. Sachant que l’échantillon étudié contient 80 % de l’acidité du vin, indiquer s’il a subi la piqûre
acétique.
Concentration massique : 0,126 x M(acide acétique) = 0,126 x60,1 ~7,6 g / L.
La
concentration en masse d’acide éthanoïque est réglementée : elle ne doit pas dépasser
0,9 g·L
–1.
Ce vin est piqué.
2. Le raisin est-il arrivé à maturité ? On souhaite savoir si le jus du raisin récolté peut être utilisé pour obtenir du vin AOC Cahors.
La concentration en masse de sucre du jus de raisin peut être déterminée par une mesure de l’indice
de réfraction du jus de raisin.
On réalise au laboratoire les mesures d’indices de réfraction de différentes solutions sucrées à des
concentrations en masse de sucre connues à l’aide d’un réfractomètre. On obtient alors une droite
d’étalonnage représentant l’indice de réfraction n en fonction de la concentration en masse Cm de
sucre donnée ci-dessous.
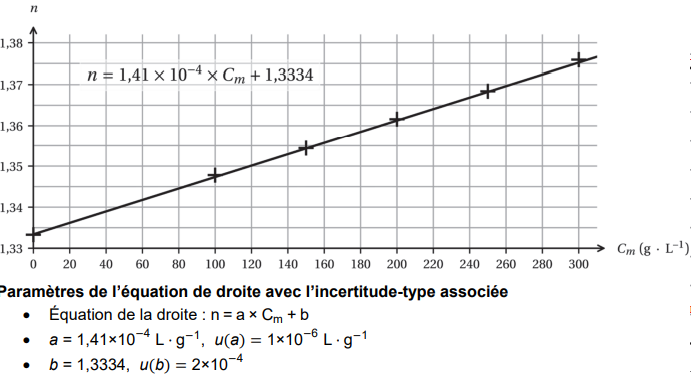
Au laboratoire, l’indice de réfraction mesuré pour le jus de raisin utilisé pour élaborer le vin a pour
valeur 1,365.
On peut utiliser un script en langage de programmation Python afin d’obtenir de nombreuses valeurs
de concentration en masse de sucre du jus de raisin.
1. Expliquer la ligne 35 du script proposé dans le document 3 en s’aidant du document 2.
La ligne 35 donne la concentration massique Cm.
2. Compléter les lignes 18 à 21 de l’extrait du script Python proposé.
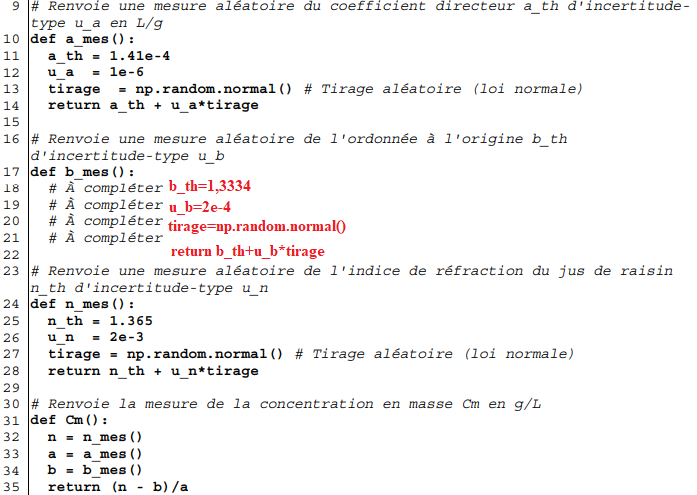
Les résultats de la simulation peuvent être visibles sur l’histogramme de distribution.
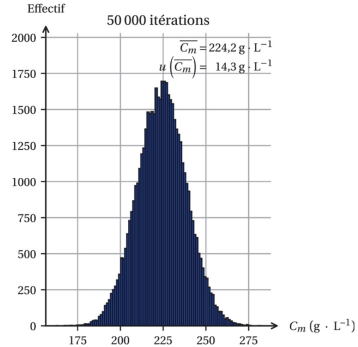 3.
3. Déterminer si le raisin récolté est à bonne maturité pour préparer le vin AOC Cahors en vous
appuyant sur l’histogramme et au vu des incertitudes.
Cm+u(c)=238,5 g/L.
Cm-u(c) =209,9 g/L.
Un jus de raisin peut être considéré comme étant à bonne maturité quand la concentration en
masse de sucre est d’au moins 180 grammes par litre de jus.
Ces valeurs étant supérieures à 180 g/ L, le raisin est à maturité.
On suppose que le degré alcoolique est proportionnel à la concentration en masse de sucre. Pour
une concentration en masse de sucre dans le jus de raisin égale à 17,0 g · L
–1
, on obtient un degré
alcoolique de 1,00 %.
4. Déterminer la valeur du degré alcoolique obtenu avec le jus de raisin étudié. Commenter le
résultat obtenu.
Cm = 224,2 g /L
224,2 / 17,0 =13,2 degrés.
Les vins rouges ayant droit à l’appellation d’origine contrôlée (AOC) « Cahors » doivent provenir
de raisins récoltés à bonne maturité et présenter un titre alcoométrique volumique naturel
minimum de 10,5 %.
Cette valeur étant supérieure à 10,5 %, le vin peut être AOC "cahors".
Fermentation du jus de raisin
Pour la production des vins rouges, le jus reste plongé dans la cuve pendant une durée d’environ
15 jours. Cette étape est exothermique, la température est maintenue entre 28 °C et 30 °C par un
système de régulation.
On va s’intéresser dans cette partie à l’étape de fermentation qui nécessite une régulation en
température.
Étude du capteur de température.
Pour mesurer la température du jus de raisin lors de l’étape de fermentation, on utilise au laboratoire
un capteur de température : une thermistance CTN (la valeur de la résistance diminue lorsque la
température augmente). Un montage utilisant un microcontrôleur sera utilisé pour mesurer la
température. Le système de mesure utilise trois DEL : une DEL rouge indique une température trop
élevée, une DEL bleue indique une température trop faible et une DEL verte indique une température
correcte.
1. Indiquer les valeurs minimale et maximale de résistance R
CTN de la CTN pour le bon
déroulement de la fermentation du jus de raisin.
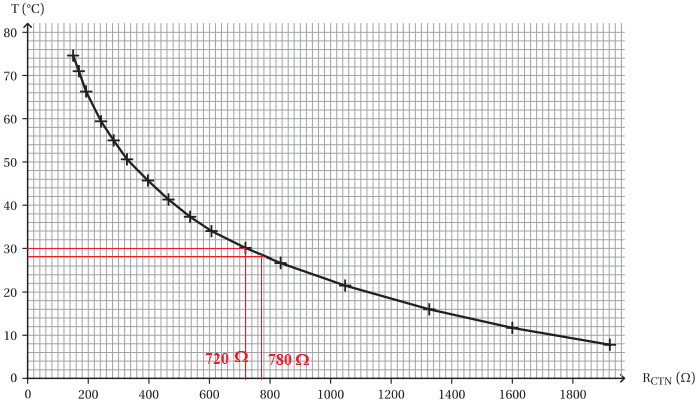 2.
2. Identifier l’entrée analogique de la carte du microcontrôleur permettant de
mesurer la tension aux bornes de la CTN.
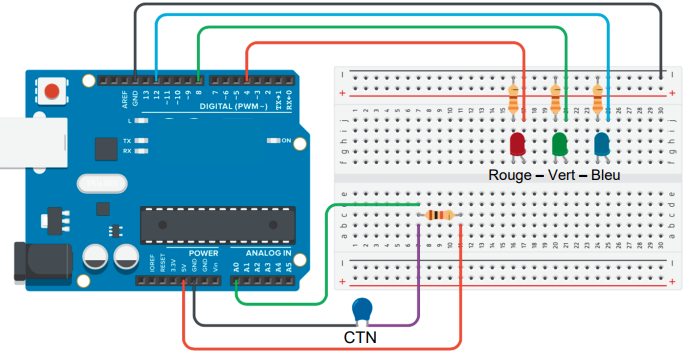 A0
A0.
3. Sachant que l’entrée analogique du microcontrôleur est codée sur 10 bits, déterminer le
nombre de valeurs binaires différentes possibles.
2
10 valeurs possibles.
4. Sachant que la tension maximale de l’entrée analogique a une valeur de 5,0 V, en déduire
le quantum du CAN (résolution de l’entrée).
q =
DU / (2
N-1)=5,0 / (2
10-1)=0,00489 V ~ 5 mV.
5. Vérifier que la valeur de la tension correspondant à une température T = 28 °C vaut 2,19 V
et que celle correspondant à une température T = 30 °C vaut 2,09 V.
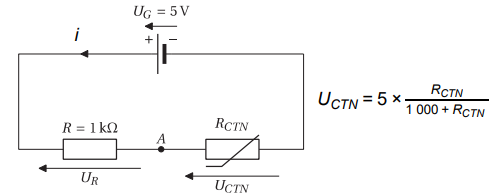
U
CTN = 5 x780 / (1000+780)=2,19 V.
UCTN = 5 x720 / (1000+720)=2,09 V.
6. Donner la signification des lignes 14, 15 et 16 du programme téléversé dans le
microcontrôleur.
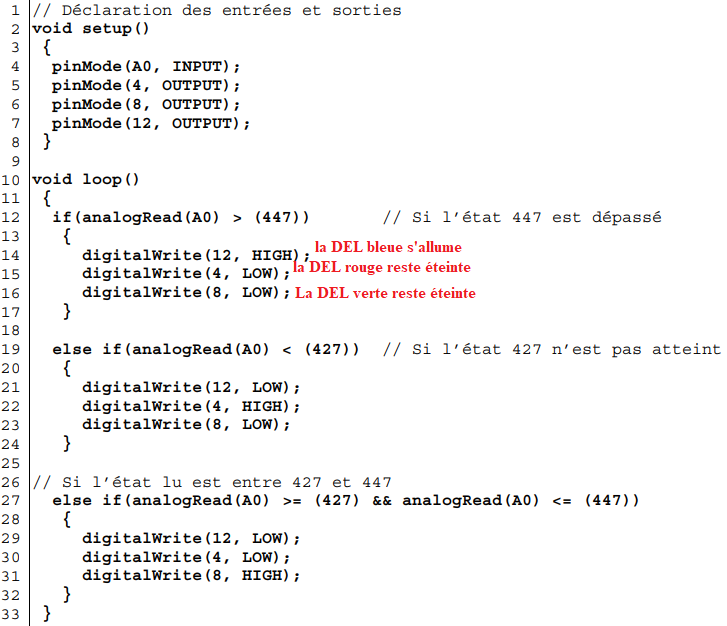 7.
7. Indiquer la couleur de la DEL allumée dans le cas où l’état lu par le microcontrôleur a pour
valeur 400.
DEL rouge allumée
8. En déduire l’état correspondant à une tension de 2,09 V à l’aide de la méthode de
votre choix.
DEL verte allumée ; système OK car codage compris entre 447 et 427.
Étude de la boucle de régulation.
On souhaite maintenant réguler la température du jus de raisin lors de la fermentation. Pour cela,
on place au laboratoire le jus de raisin dans un bain thermostaté équipé d’une résistance chauffante.
La température ambiante du laboratoire est de 20 °C.
9. Préciser les trois critères de performance d’une boucle de régulation.
La précision est évaluée par l'écart statique ;
La rapidité est évaluée par le temps de réponse.
La stabilité est évaluée par le premier dépassement.
10. Indiquer la grandeur réglée, la grandeur réglante et une grandeur perturbatrice parmi les 5
propositions suivantes :
- couleur de la DEL allumée ;
- puissance de la résistance chauffante ;
- température ambiante ;
- température du bain thermostaté ;
- tension d’alimentation du microcontrôleur.
Grandeur réglée : tension d'alimentation du microcontrôleur.
Grandeur réglante : couleur de la dEL allumée.
Grandeur perturbatrice :
température du bain thermostaté.