|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Le but de cet exercice est l'ťtude de la rťaction de saponification obtenue en mťlangeant ŗ t=0, 250 mL d'une solution d'ťthanoate de sodium CH3COO-C2H5 de concentration c1 = 10 mmol/L avec 250 mL d'une solution d'hydroxyde de sodium de mÍme concentration. Mťthode de suivi de l'ťvolution de la rťaction : La rťaction est lente ; la concentration en ion hydroxyde [HO-] dans le milieu diminue au cours du temps. On travaille dans un bain thermostatť pour maintenir la tempťrature constante. DŤs que le mťlange rťactionnel est rťalisť on soutire 8 ťchantillons de mÍme volume V= 10 mL et on laisse ťvoluer ces 8 ťchantillons identiques. A la date t1 = 2 min, on dose par une solution d'acide chlorhydrique l'ťchantillon nį1, ŗ la date t2 = 4 min, un second..... A la date du dosage ( juste avant de rťaliser celui-ci ) on ajoute des glaÁons. Dosage de l'ion hydroxyde ŗ la date t : On effectue un dosage
colorimťtrique des ions hydroxydes par une solution d'acide
chlorhydrique de concentration c2 = 1,0 10-3
mol/L.
Dosage des ions hydroxyde :
Cinťtique :
corrigť Rťaction de saponification : Equation de la rťaction de saponification : CH3COO-C2H5 + HO- ---> CH3COO- + C2H5OH Noms des produits obtenus : ion ťthanoate ( acťtate) et ťthanol Ces caractťristiques : lente mais totale Quantitť initiale d'ion hydroxyde et la concentration initiale [HO-]0 : V1=250 mL d'une solution d'hydroxyde de sodium de concentration c1 = 10 mmol/L. n(HO-)
= V1 c1 = 0,25* 10 10-3
= 2,5 10-3 mol dans un volume final de 0,5 L ; [HO-]0 = 2,5 10-3
/0,5 = 5 10-3 mol/L = 5 mmol/L
Les deux bases prťsentes dans le milieu rťactionnel sont : HO- et CH3COO- Equations relatives aux rťactions de ces bases avec l'ion oxonium H3O+ : HO- + H3O+ = 2H2O ; K1= 1/([HO-][H3O+]) = 1/10-14 = 1014. CH3COO- + H3O+ = H2O + CH3COOH ; K2= [CH3COOH] / ([H3O+][CH3COO-]) or Ka = [CH3COO-][H3O+]/[CH3COOH] d'oý : K2=1/Ka = = 1/ 10-4,75 = 104,75 = 5,6 104. K2<<K1 donc la rťaction qui se produit en premier ( rťaction de dosage) est celle mettant en jeu les ions hydroxydes. L'ťquivalence de cette rťaction est obtenue pour un volume d'acide Vťq versť. ŗ l'ťquivalence : C2Vťq = [HO-]V ; [HO-] =C2Vťq /V=10-3Vťq /10 = 10-4Vťq mol/L = 0,1 Vťq mmol/L avec Vťq en mL
Un des produits formťs lors de la rťaction est de l'ťthanol ; Relation donnant la concentration en ťthanol en fonction de la concentration en ion hydroxyde : La quantitť de matiŤre (mol) d'ion hydroxyde disparu est ťgale ŗ la quantitť de matiŤre (mol) formť : [ťthanol]t=[HO-]0 -[HO-]t.
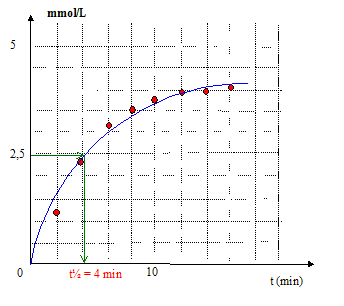
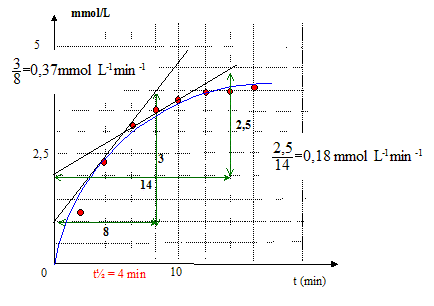
la limite de la courbe : le mťlange initial est stoechiomťtrique ; au bout d'un temps trŤs long, la rťaction ťtant totale, la concentration en ťthanol sera : 5 mmol/L le temps de demi-rťaction tĹ : temps au bout duquel l'avancement est ťgal ŗ la moitiť de l'avancement final Ĺtfin = 2,5 mmol d'ťthanol Vitesse volumique intantanťe de la rťaction : v = 1/V dx/dt =d[ťthanol]/dt coefficient directeur de la tangente ŗ la courbe ŗ la date considťrťe.
Composition du systŤme ŗ t = 2tĹ= 8 min [ťthanol]=[CH3COO-]= 3,5 mmol/L ; [HO-] =[ester]=1,5 mmol/L la vitesse diminue au cours du temps : la concentration des rťactifs est un facteur cinťtique ; celle-ci diminue au cours du temps.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Principe : L'acide acťthylsalicylique est prťparť par rťaction entre l'acide salicylique et l'anhydride ťthanoÔque en prťsence d'acide sulfurique, selon la rťaction : HO-C6H4-COOH + CH3-CO-O-CO-CH3 ---> CH3-CO-O-C6H4-COOH + CH3-COOH Etape 1 : On prťpare un bain marie (50 - 60įC). Dans un erlenmeyer bien sec, on introduit successivement avec prťcaution 10,0 g d'acide salicylique, 15 mL d'anhydride ťthanoÔque mesurťe avec une ťprouvette graduťe, 5 gouttes d'acide sulfurique concentrť. On adapte un rťfrigťrant ŗ boules sur l'erlenmeyer, puis on agite le mťlange et on place l'erlenmeyer dans le bain-marie pendant 0,25 heure en agitant. Etape 2 : On retire l'erlenmeyer du bain-marie et on le refroidit lťgťrement sous un filet d'eau du robinet. On enlŤve le rťfrigťrant et on ajoute 50 mL d'eau froide. On ajoute 50 mL d'eau glacťe et on refroidit l'erlenmeyer dans la glace. On filtre le mťlange sur bŁchner et on rince les cristaux avec de l'eau glacťe. On les pŤse aprŤs sťchage et on trouve une masse de 10,68 g. Chromatographie :
corrigť Composť chimique utilisable ŗ la place de l'anhydride ťthanoÔque : l'acide ťthanoÔque CH3-COOH Equation bilan : HO-C6H4-COOH + CH3-COOH = CH3-CO-O-C6H4-COOH + H2O Justifions le choix initial : dans le cas de l'acide ťthanoÔque la rťaction est lente, limitťe par l'hydrolyse de l'ester. rŰle de l'acide sulfurique concentrť : catalyseur l'erlenmeyer dit Ítre sec car l'anhydride ťthanoÔque rťagit rapidement avec l'eau pour donner l'acide ťthanoÔque. Quantitťs de matiŤre initiales des deux rťactifs : anhydride ťthanoÔque : masse (g) =volume (mL) * densitť =m = 15*1,08 = 16,2 g M =4*12+6+3*16=102 g/mol n= m/M= 16,2 / 102 = 0,16 mol acide salycilique : M=7*12+6+3*16 =138 g/mol ; n=m/M = 10 / 138 = 7,2 10-2 mol ( en dťfaut) Le rťactif limitant est l'acide salicylique ; on peut espťrer obtenir au plus 7,2 10-2 mol d'ester. masse thťorique d'ester :7,2 10-2 M(ester) = 7,2 10-2*180= 13 g. Rendement de la synthŤse : masse expťrimentale / masse thťorique *100 = 10,68 /13*100 = 82%. Nom de l'ťtape 2 : blocage cinťtique Chromatographie : composition de l'aspirine prťparťe : acide
acťthylsalycique
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|