|
D'aprŤs
concours Fesic (
chimie) 2006
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts.
|
|
.
.
|
|
|
|
rťpondre
vrai ou faux.
Masses atomiques molaire en g/mol : H : 1 ; C
: 12 ; O : 16 ; Na : 23 ; Cd : 112,4 ; Ni : 58,7.
- On mesure l'absorbance d'une solution de sulfate de
cuivre ( Cu2++ SO42-)
a) L'absorbance augmente avec la concentration molaire en solutť
apportť de la solution. vrai
b) La courbe reprťsentant l'ťvolution de
l'absorbance A avec la concentration molaire en solutť apportť est une
droite pour les faibles concentrations. vrai
c) L'absorbance ne dťpend pas de la longueur
d'onde de la lumiŤre utilisťe. faux
Une solution
de concentration molaire en solutť apportť c1=0,100
mol/L a une absorbance A1=0,30. Une solution de
concentration molaire en solutť apportť c2=0,050
mol/L a une absorbance A2=0,15.
d) Le mťlange ŗ volume ťgal de ces deux
solutions a une absorbance A=0,45. faux. Mťlangeons 500 mL de chaque
solution ; n(Cu2+) = Ĺ (c1+c2)
dans 1 L de mťlange ; concentration et absorbance ťtant
proportionnelles, d'oý l'absorbance A du mťlange A= Ĺ(A1+A2).
- On On rťalise
l'ťtude cinťtique de la transformation des ions peroxodisulfate par les
ions iodure. Le mťlange rťactionnel est rťalisť avec un volume V1=25,0
mL de solution de peroxodisulfate de potassium de concentration molaire
en solutť apportť c1 = 5 mmol/L et un volume V2
de solution d'iodure de potassium de concentration molaire en solutť
apportť c2 = 0,250 mol/L, de sorte que l'un des
rťactifs soit en large excŤs.
L'ťquation bilan s'ťcrit : S2O82-
+ 2I-= 2SO42-+I2.
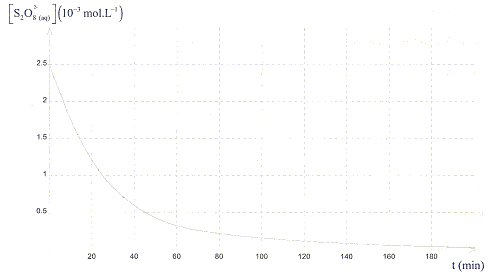
Un graphe indiquant la variation de la concentration molaire en ions S2O82-
en fonction du temps a ťtť tracť :
a) l'ion
peroxodisulfate joue le rŰle d'oxydant. vrai.
b) L'ion iodure est le rťactif limitant. faux.
D'aprŤs le graphe, ŗ t >180min [S2O82-
] est nulle ; S2O82-
est le rťactif limitant.
c) V2=25 mL. vrai (
lecture graphe) [S2O82-
]0 = 2,5 10-3 mol = 2,5
mmol = C1V1/(V1+V2)
; V1+V2
= 5 *25/2,5 = 50 mL ; V2 =25 mL.
d) Le temps de demi rťaction est lťgťrement infťrieur ŗ 20 min. vrai
lecture graphe pour [S2O82-
] =Ĺ[S2O82-
]0 =1,25 10-3 mol/L.
|
|
- L'eau de Javel est dťsinfectant, elle est
fabriquťe en solution aqueuse selon la rťaction quasi-totale : Cl2(g)
+ 2HO- = ClO- + Cl-
+ H2O. (1)
Le degrť chloromťtrique (įCHl) est le volume exprimť en L de dichlore
gazeux qui a ťtť utilisť pour prťparer un volume de 1,00 L d'eau de
Javel. Vm=22,4 L/mol. On considŤre de l'eau de
Javel ŗ 48,0įCHl.
a) Dans ces conditions, 60 L de dichlore gazeux sont
nťcessaires pour prťparer 500 mL d'eau de Javel. faux. 48įCHl soit 48
L de dichlore pour prťparer 1L ou 24 L de dichlore pour prťparer ĹL.
b) La concentration molaire en ion hypochlorite ClO-
est environ ťgale ŗ 2,1 mol/L. vrai.
n(Cl2) = 48/22,4 = 2,1
mol dans 1 L ; de plus n(Cl2) =n(ClO-).
La teneur en ion hypochlorite diminue au cours du temps car les ions se
transforment lentement en ion chlorure avec dťgagement de dioxygŤne
suivant la rťaction : ClO- = Cl-+ĹO2
(2). On ťtudie la cinťtique de cette dťcomposition.
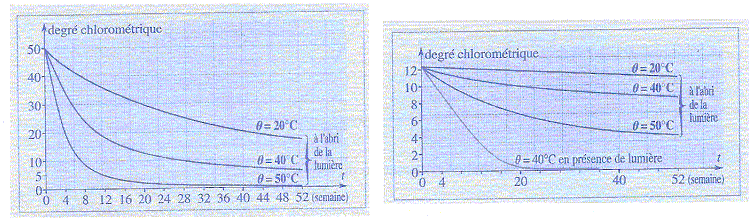
c) La tempťrature et l'absence de lumiŤre sont deux
facteurs cinťtiques qui font ťvoluer le systŤme dans le mÍme sens. faux.
si la tempťrature augmente la vitesse de la rťaction
augmente ; ŗ la lumiŤre la rťaction est plus rapide
pour une mÍme tempťrature.
Lors de sa fabrication un berlingot d'eau de Javel contient 0,50 mol
d'ion hypochlorite. Lors de son utilisation, 6 mois plus tard, il ne
contient plus que 0,48 mol. Le volume d'un berlingot est 250 mL
d) La vitesse moyenne volumique de la rťaction nį2 est ťgale ŗ 3 mol L-1
mois -1. faux.
diminution de 0,08 mol par litre en 6 mois soit
0,08/6 =0,013 mol L-1 mois -1.
- On rťalise le mťlange de V1=20,0
mL de permanganate de potassium de concentration molaire en solutť
apportť C1=2,00 10-3
mol/L et V2 = 20,0 mL d'acide oxalique HOOC-COOH
( solution incolore) de concentration molaire en solutť apportť C2
= 5,00 10-2 mol/L. La rťaction mise en jeu est
lente et considťrťe comme totale, son ťquation est : 2 MnO4-
+ 5 H2C2O4
+ 6H+ = 2Mn2+ + 8H2O+
10 CO2.
On suit son ťvolution par spectrophotomťtrie. On mesure l'absorbance A
du mťlange rťactionnel placť dans la cuve du spectrophotomŤtre. Dans
ces conditions, la concentration molaire en ion permanganate est
proportionnelle ŗ la valeur de l'absorbance A. L'absorbance A(t) et
l'avancement de la rťaction x(t) sont reliŤs par la relation : x(t) =
(2 10-5 -A(t) 10-5) mol.
Par un logiciel appropriť on obtient la courbe suivante :
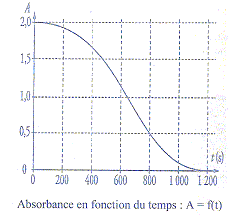
a) L'un des couples
d'oxydorťduction mis en jeu dans la rťaction chimique est CO2/H2C2O4.
vrai.
b) Le temps de demi rťaction est ťgale ŗ 650 s. vrai. ŗ tĹ
l'avancement est ťgal ŗ la moitiť de l'avancement
final ; Afin =0 d'oý xfin
=2 10-5 mol ;
xtĹ= 10-5 mol d'oý AtĹ=1
; puis lecture graphe : tĹ voisin 650 s.
On recommence l'expťrience prťcťdente en prenant le mÍme volume V2
d'une nouvelle solution d'acide oxalique de concnetration molaire en
solutť apportťe C'2 = 2,50 10-3
mol/L
c) La solution finale n'est plus incolore. vrai.
n(MnO4-)0
= C1V1 = 40 10-3
mmol ; n(H2C2O4)0
= C'2V2 = 50 10-3
mmol ;
ŗ partir de 50 10- 3 mmol d'acide oxalique on
consomme 50 10- 3 /2,5 = 20 10-3
mmol d'ion permanganate ; ce dernier est en excŤs de 20 10-3
mmol.
d) L'absorbance finale vaut 1.vrai
La quantitť de matiŤre finale d'ion permanganate est
ťgale ŗ la moitiť de la quantitť initiale de cet ion ; l'absorbance
initiale vaut 2 ; volume constant ; ; absorbance et concentrations sont
proportionnelles.
- On prťpare une solution aqueuse ŗ 5 10-3
mol/L d'acide mťthanoÔque. La conductivitť de la solution, mesurťe ŗ 25
įC a pour valeur s= 3,3
10-2 S/m.
Donnťes : 4,05*8,1 = 33. l(H3O+)=35
10-3 S m≤ mol-1 ; l(HCOO-)=5,5
10-3 S m≤ mol-1.
a) L'ancien nom de l'acide mťthanoÔque est acide acťtique. faux.
b) Les ions mťthanoate et les ions oxonium sont quasiment en mÍme
quantitť dans la solution. vrai .
La
solution est ťlectriquement neutre : [HCOO-]+ [HO-]=[H3O+]
et [HO-] nťgligeable en milieu acide.
c) [H3O+]
= 0,81 mmol/L. vrai
s = l(H3O+)[H3O+]
+ l(HCOO-)[HCOO-]=(
l(H3O+)+l(HCOO-))[H3O+]
; [H3O+]=3,3
10-3 /((35+5,5)10-3)=3,3/40,5
=0,81 mol m-3 = 0,81 mmol/L
d) Le
taux d'avancement de la rťaction est ťgal ŗ 16 %. vrai
[H3O+]
= t c ; t =[H3O+]
/c = 0,81 10-3 / 5 10-3
= 0,81/5 = 0,0162 soit 16,2%.
|
|
acide
base
- L'acide borique H3BO3
est utilisť comme antiseptique en solution aqueuse, par exemple dans
les collyres. On considŤrera ici qu'il s'agit d'un monoacide. On
souhaite rťaliser un dosage pH-mťtrique de 20 mL d'une solution de cet
acide par une solution d'hydroxyde de sodium. La solution titrante a
une concentration de 1,0 10-2 mol/L. On obtient
les courbes suivantes pH=f(V) et dpH/dV= g(V).
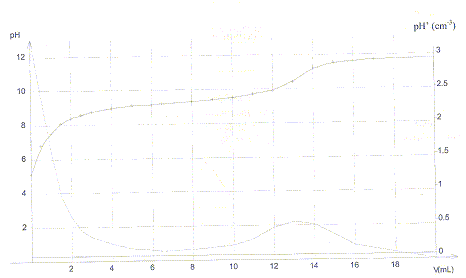
a) La base conjuguťe de l'acide borique est BO2-.
faux H2BO3-.
b) On peut ťgalement dťtecter l'ťquivalence avec la phťnolphtalťine
dont la zone de virage se situe entre pH=8,2 et pH=10. faux. le pH du point
ťquivalent pH voisin de 11 n'appartient pas ŗ la zone de virage de cet
indicateur..
c) D'aprŤs le graphe le pKa de l'acide borique est compris entre 8 et10.vrai
pKa = pH ŗ la demi-ťquivalence soit pour un volume
de soude voisin de 6,5 mL.
d) La concentration molaire de la solution d'acide borique a une valeur
proche de13 10-3 mol/L.faux
volume ťquivalent : 13 mL d'oý C = 13*0,01 / 20 =
6,5 10-3 mol/L.
- Une espŤce chimique A rťagit sur une espŤce chimique
B. L'ťquation de la rťaction est modťlisťe par : aA+bB=cC+dD. Le
diagramme d'ťvolution thťorique des quantitťs de matiŤre des rťactifs
est reprťsentť ci-dessous :
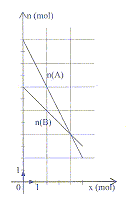
a) Les nombres stoťchiomŤtriques a et b sont dans le
rapport a/b=2. vrai.
les valeurs absolues des coefficients directeurs des
droites n(A) = f(x) et n(B) = g(x) donnent a=2 et b=1.
b) L'espŤce B est le rťactif limitant. faux.
n(A) = f(x) couperait la premiŤre l'axe des
abscisses.
c) L'avancement maximal est ťgal ŗ 4 mol. faux.
|
avancement (mol)
|
aA
|
+bB
|
=cC
|
+dD
|
|
initial
|
0
|
12
|
8
|
0
|
0
|
|
en cours
|
x
|
12-ax = 12-2x
|
8-bx=8-x
|
cx
|
dx
|
|
fin
|
xmax = 6 mol
xfin = 5 mol
|
12-2xmax=0
|
8-xmax = 2 mol
|
cxmax
|
dxmax
|
d) Le taux d'avancement final est voisin de
t = 0,8. faux
t = xfin
/xmax = 5/6 .
- On considŤre la rťaction d'autoprotolyse de l'eau
Ke(25) = 1,0 10-14 ; Ke(60) = 1,0 10-13
ŗ 60įC.
Donnťes : NA= 6,02 1023 mol-1
; masse volumique de l'eau = 1 g/mL ŗ 25įC
a) L'eau est un ampholyte. vrai.
elle peut jouer le rŰle d'acide ou le rŰle de base.
b) Il y a plus de molťcules d'eau dissociťes en ions ŗ 60įC qu'ŗ 25įC. vrai. Ke(60)
> Ke(25)
c) Dans 1 L d'eau ŗ 25įC il y a 6,0 1016
molťcules d'eau dissociťes en ions. vrai.
10-7 mol dion oxonium ; donc
10-7 mol de molťcules d'eau dissociťes soit 10-7
*6,02 1023 =6,02 1016
molťcules d'eau dissociťes.
d) ŗ 60įC une solution de pH=7 est acide. faux
ŗ 60įC le milieu neutre a un pH ťgal ŗ 6,5 ; pH=7
est un milieu basique.
- L'ťthylamine C2H5NH2
est une base de BrŲnsted. L'acide conjuguť est l'ion ťthylammonium C2H5NH3+.
On prťpare une solution aqueuse d'ťthylamine ŗ 0,020 mol/L. Le pH de
cette solution vaut 11,9.
Donnťes : pKa( C2H5NH3+
/C2H5NH2
)= 10,7 ; log 5,0 10-4 = -3,3 ; log 5,0 10-13
= -12,3 ;
a) l'ťthylamine possŤde un isomŤre. vrai. CH3-NH-CH3.
: dimťthylamine
b) l'ťthylamine est complťtement dissociťe dans l'eau. faux ; sinon le pH de
la solution serait ťgal ŗ 14+log0,01 = 12 ; or on mesure une valeur
infťrieure ŗ 12.
c) La constante de rťaction de l'ťthylamine avec l'eau est ťgal ŗ K=
5,0 10-4. vrai
C2H5NH2
+ H2O = C2H5NH3+
+ HO- ; K= [C2H5NH3+][HO-
]/[C2H5NH2]
; or Ka =[C2H5NH2][H3O+]/
[C2H5NH3+]
;
K=Ke/Ka = 10-14 / 10-10,7
= 10-3,3 = 5,0 10-4
d) On dose 20 mL de la solution d'ťthylamine par une solution d'acide
chlorhydrique ŗ 0,025 mol/L. Le
volume ťquivalent est: VE=16 mL. vrai
20*0,02 =0,025 VEsoit
VE=16 mL .
- Le calcaire CaCO3 peut se
dissoudre en prťsence de CO2. l'ťquation de la
rťaction s'ťcrit : CaCO3 (s)+ CO2
+H2O = 2HCO3-+Ca2+.
La constante d'ťquilibre de cette rťaction est K= 3,5 10-6.
a) L'expression de la constante est K= [HCO3-]ťq≤[Ca2+]ťq
/[CO2]ťq. vrai.
Les concentrations molaires initiales sont : [HCO3-]0=8,0
10-4 mol/L ; [Ca2+]0
=3,8 10-4 mol/L ;[CO2]0=1,0
10-2 mol/L.
b) Le quotient de rťaction initial vaut Qr i =
3,0 10-5. faux.
Qr i =(8,0 10-4)2
*3,8 10-4 / 1,0 10-2 =2,4
10-8.
c) Dans ces conditions le calcaire se dissout. vrai.
Qr i < K donc
ťvolution dans le sens direct.
d) Le pH de la solution initiale vaut 7,5. faux.
Donnťes : pH=pKa + log([base]/[acide] ; 8,0*3,8 =30 ; 8,02*3,8 = 240 ;
log (1/8 10-2)=1,1 ; log 8 10-2 = -1,1 ;
pKa (CO2 ,H2O / HCO3-
) = 6,4
log ([HCO3-]0
/ [CO2]0 )=log(8
10-4 / 10-2) =-1,1 ; pH=
6,4-1,1 = 5,3).
|
|
Pile-
ťlectrolyse
- Un dentiste pose une couronne en or ŗ cŰtť d'une
couronne en acier ( alliage fer carbone contenant une grande proportion
de fer). Il se forme alors une pile schťmatisťe de la faÁon suivante :
Fe(s) / Fe2+(aq) //H+
(aq)/H2(g). L'ťlectrode constituťe par la
couronne d'or reste inaltťrťe et le couple en jeu ŗ cette ťlectrode est
le couple H+ (aq)/H2(g).
de nombreuses boissons jouent le rŰle de solutions ťlectrolytiques.
a) La couronne d'acier va Ítre rapidement fragilisťe
par la rťaction d'oxydation du fer, la manipulation du dentiste n'est
pas judicieuse. vrai.
b) La couronne d'or constitue le pŰle positif de cette pile. vrai. rťduction de H+,
donc cathode positive.
On considŤre maintenant une pile classique formťe d'une ťlectrode
inattaquable plongeant dans 100 mL d'une solution acide ŗ C= 0,100
mol/L et d'une ťlectrode de fer en large excŤs, plongeant dans une
solution de nitrate de fer de concentration molaire C.
On considŤre la rťaction Fe(s) = 2H+(aq) = Fe2+(aq)
+ H2(g) dont la constante d'ťquilibre a pour
valeur K= 2 1015 ŗ 25įC.
AprŤs calcul, le quotient de rťaction dans l'ťtat initial vaut Qr
i = 1/C.
c) Le systŤme ťvolue dans les sens inverse de la rťaction considťrť. faux. Qr i
= < K, ťvolution dans le sens direct.
d) La charge transfťrťe au cours de l'ťvolution du systŤme vaut 965 C. vrai n(H+)
=0,01 mol ; or H++e- = ĹH2
donc n(e-) = 0,01 mol ;
Q= 96500*0,01 = 965 C.
- Le nickel mťtallurgique obtenu ŗ partir du minerai
contient des impuretťs. On le purifie par ťlectrolyse. L'ťlectrolyte
utilisť est du sulfate de nickel. L'une des ťlectrode A est une plaque
de nickel ŗ purifier. L'autre B est une plaque de nickel pur. Pendant
l'ťlectrolyse, le nickel contenu dans A s'oxyde et disperse ces
impuretťs dans la solution ťlectrolytique. La rťaction qui a lieu dans
l'ťlectrolyseur est : Ni(s) + Ni2+(aq) = Ni(s) +
Ni2+(aq)
Le gťnťrateur dťbite un courant d'intensitť I= 2,0 A constant sous une
tension U= 4,0 V pendant 5,0 h.
Donnťes : 965/36=27.Ni : 58,7 g/mol
a) Le nickel impur constitue l'anode. vrai.
anode = "oxydation " du mťtal impur.
b) Les cations se dťplacent vers la cathode. vrai.
c) L'avancement de la rťaction au bout de 5 h est de 0,050 mol. faux. Q=It = 2*5*3600
= 36 000 C ; Q= 96 500 n(e-) ; n(e-)
= 36000/96500 = 360/965=10/27 = 0,373 mol d'ťlectrons ; or
Ni(s) = Ni2+(aq) + 2 e- ;
avancement x =n (Ni2+) = Ĺ n(e-)
= 5/27 =0,186 mol .
d) L'expťrience permet de dťposer une masse de nickel pur supťrieure ŗ
8,0 g. vrai. n
(Ni) = Ĺ n(e-) = 5/27 ; masse
= nM = 5/27*58,7 = 10,9.
- Le cadmium mťtallurgique est produit industriellement
par ťlectrolyse d'une solution acidifiťe de sulfate de cadmium II.
Cette ťlectrolyse est rťalisťe sous une tension de 3,1 V. On considŤre
un ťlectrolyseur qui produit 1 tonne de cadmium en 24 h. Couples redox
: Cd(s) / Cd2+(aq) ; H+(aq)
/H2(g) ; O2(g) / H2O(l).
96,5/ (112,4*24*36) = 10-3.
a) L'ťlectrode oý se forme le cadmium est reliťe ŗ la borne nťgative du
gťnťrateur. vrai. cathode
nťgative = " rťduction " des ions cadmium.
b) Il se forme du dihydrogŤne ŗ l'anode. faux.
anode = "oxydation " de l'eau en dioxygŤne.
c) Il se forme du dioxygŤne ŗ l'anode. vrai
.
d) L'intensitť du courant vaut 25 000 A. faux.
n(Cd) = m/M = 106/112,4 mol ;
or Cd2+ + 2e- = Cd(s)
d'oý n(e-) =2*106/ (112,4)
Q= 96500 n(e-) = It soit I= 96500 n(e-)
/ t = 2*96500 106/ (112,4*24*3600) =
96,5/ (112,4*24*36) *2 107 = 2104
= 2 104A.
|
|
chimie
organique
- Une huile alimentaire est constituťe d'un
triglycťride appelť olťine (M= 884 g/mol) dont la formule semi
dťveloppťe est :
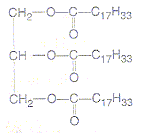
On chauffe ŗ reflux un mťlange constituť de 88,4 g
d'olťine, 100 mL d'ťthanol, une solution d'hydroxyde de sodium en
excŤs. AprŤs 25 min on laisse refroidir le contenu du ballon, puis on
verse celui-ci dans 250 mL d'une solution saturťe en chlorure de
sodium. On filtre sur bŻchner et on rince le savon obtenu ŗ l'eau
froide. On prťpare une solution d'eau savoneuse en disolvant des
copeaux de savon dans un peu d'eau.
a) L'un des produits de la rťaction est le glycťrol.
vrai.
b) La solution saturťe de chlorure de sodium permet d'ťliminer la soude
en excŤs. faux. relargage,
prťcipitation du savon.
c) La rťaction produit 91,2 g de savon. vrai.
n (olťine) = 88,4/884 = 0,1 mol donc 0,3 mol de
savon ( olťate de sodium C17H33COO
Na : M= 304 g/mol) ; masse de savon = nM = 0,3*304 =91,2 g .
d) Un papier pH trempť dans l'eau savonneuse rťvŤle un pH basique. vrai. prťsence d'une
base, l'ion olťate C17H33COO-.
- L'eugťnol extrait de l'huile essentielle des clous de
girofle est utilisť dans certains produits des domaines mťdical et
dentaire en raison des propriťtťs entalgiques et antiseptiques.
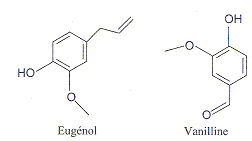
a) La vanilline est un ester de l'eugťnol. faux.
b) La vanilline possŤde une fonction aldehyde. vrai.
groupe carbonyl >C=O en bout de chaine.
c) La molťcule ci-dessous est l'acťtate d'eugťnyle
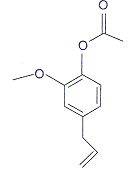 vrai. vrai.
d) On rťalise l'estťrification par l'acide acťtique
d'une mole d'eugťnol et, aprŤs extraction, on rťcupŤre 103 g d'acťtate
d'eugťnyle. Le rendement de la
rťaction est 50%. vrai.
M( eugťnol) = 12*10+12+32=154 g/mol ; M ( acťtate
d'eugťnyle) =12*12+14+48=206 g/mol ; on peut obtenir au maximum 1 mol
d'ester soit 207 g.
- A 25įC on ťtudie par conductimťtrie la cinťtique de
l'hydrolyse basique d'un ester RCOOR'. La quantitť de soude introduite
est 10 mmol. L'ester est en excŤs. En fin de rťaction, la conductance Gf
de la solution est 9,1 mS. Le mťlange rťactionnel est trŤs diluť.
|
ion
|
l en
S m≤ mol-1
|
|
H3O+
|
3,5 10-2
|
|
HO-
|
2,0 10-2
|
|
Na+
|
5,0 10-3
|
|
RCOO-
|
4,1 10-3
|
a) Il s'agit d'une rťaction totale. vrai.
b) La conductivitť du mťlange rťactionnel augmente au cours du temps. faux. du point de
vue de la conductimťtrie, on remplace HO- par
RCOO- de conductivitť molaire ionique beaucoup
plus faible.
c) L'avancement final est xf = 10 mmol. vrai. soude en dťfaut.
d) La conductance initiale de la solution est G0
= 25 mS. vrai.
G0 = l(HO-)[HO-]+l(Na+)[Na+] =(l(HO-)+l(Na+))[HO-]0 =
2,5 10-2[HO-]0 =
2,5*10 10-5/V ;
G=l(Na+)[Na+]+l(RCOO-)[RCOO-] =(l(RCOO-)+l(Na+))[RCOO-]f
=9,1 10-3[RCOO-]f =9,1*10
10-6/V = 9,1 10-3
S d'oý V=10-2 m3 ;
G0 =2,510-4/10-2
=25 mS
|
|
retour
-menu
|







 vrai.
vrai.