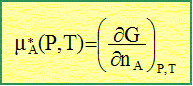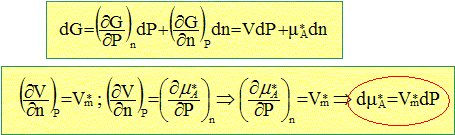|
Montťe de la sŤve dans les arbres ; pression osmotique concours agrťgation 2007 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
||||
| .
. |
||||
|
||||
|
On s'intťresse ici ŗ la montťe de la sŤve dans les arbres. Pression osmotique. On considŤre un rťcipient formť de deux compartiments, gauche et droite, de mÍme volume V et de mÍme tempťrature T, sťparťs par une membrane semi-permťable, c'est ŗ dire permťable au solvant A mais impermťable ŗ un solutť B. Le compartiment de gauche contient une solution supposťe idťale du solutť B dans A, celui de droite le solvant pur sous la pression P. Rappeler la dťfinition du potentiel chimique mA*(P,T) du corps pur A ŗ la pression P et ŗ la tempťrature T. On note G(P,T, nA) la fonction d'ťtat enthalpie libre associťe ŗ A, corps pur.
A partir de l'expression de la variation d'enthalpie libre dG, exprimer la variation dmA* du potentiel chimique du corps pur A en fonction du volume molaire Vm* de A et de la variation de pression dP qui en est la cause ŗ tempťrature T fixťe. dG= V dP-SdT+mA*dnA A tempťrature constante le terme SdT est nul : dG= V dP+mA*dnA. On note n= nA.
On supposera par la suite que Vm* ne dťpend pas de la pression. Donner l'expression du potentiel chimique du solvant A dans chaque compartiment. Compartiment de droite : le solvant est pur : mA droite = m A*(P,T). Compartiment de gauche : on note xA la fraction molaire de A et P' la pression dans ce compartiment : mA gauche = m A*(P',T) + RT ln xA. Le systŤme est ŗ l'ťquilibre. Ecrire la condition d'ťquilibre que doit vťrifier le solvant. mA droite =mA gauche m A*(P,T) = m A*(P',T) + RT ln xA. m A*(P',T) -m A*(P,T) = -RT ln xA. m A*(P',T) -m A*(P,T) = dm A* = Vm*dP = Vm*(P'-P) On note p= P'-P p= -RT / V*m ln xA. Or xA<1 donc ln xA<0 et -RT ln xA>0 donc pest positif. Il existe une surpression p ( pression osmotique) dans le compartiment de gauche.
Montrer que la pression osmotique est de la forme p=nBRT/ V oý nB est la quantitť de matiŤre du solutť B. xA+ xB = 1 soit - ln xA =- ln(1-xB) Si xB <<1 alors - ln(1-xB) voisin de xB. d'oý p = RT / V*mxB. xB = nB/(nA+nB) En solution diluťe ( nB<<nA), xB voisin de nB/nA. d'oý p = RT nB /(nAV*m). En solution diluťe nAV*m voisin Vdroite voisin Vgauche = V. Par suite : p = RT nB /V.
A.N : cas de la sŤve d'ťrable. On prendra T= 290 K; masse volumique de la sŤve : rsŤve = 103 kg m-3. La concentration du sucre dans une sŤve normale , assimilťe ŗ une solution aqueuse, est environ C=10 g/L. Calculer la pression osmotique de la sŤve par rapport ŗ l'eau du sol autour des racines. nB/V =C/M avec M : masse molaire du saccharose C12H22O11. M = 12*12+22+16*11 = 342 g/mol. nB/V = 10/342 = 2,92 10-2 mol/L = 29,2 mol m-3. p = RT nB /V. p = 8,32*290* 29,2 = 7,05 104 Pa = 0,70 bar.
p = rsŤve g h. h = p / ( rsŤve g) = 7,05 104 / (103*9,8) =7,2 m. La pression osmotique peut-elle expliquer la montťe de la sŤve dans les grands arbres ( hauteur supťrieure ŗ 20 m) ? Non, c'est l'ťvapotranspiration au niveau des feuilles. Sous l'action de la chaleur solaire, les feuilles transpirent : l'eau contenue dans les feuilles s'ťvapore. Cette ťvaporation entraÓne une dťpression dans les canaux qui transportent la sŤve : il en rťsulte un effet de succion dans les racines.
|
||||
|
|
||||
|
|