|
Pile
et appareils nomades : piles ŕ hydrogčne,
radioactivité,
condensateur
bac S France septembre
2008. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts. |
||||||||
|
||||||||
|
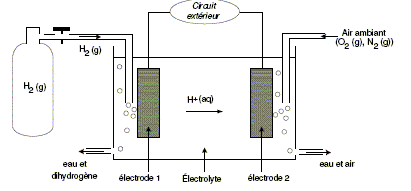
La pile ŕ hydrogčne présente des avantages importants en termes d’environnement (rejets non polluants au cours de son utilisation et absence de nuisance sonore). Elle est constituée de deux électrodes ŕ la surface desquelles ont lieu les réactions chimiques d’oxydoréduction et d’un électrolytedans lequel se déplacent les ions.
Au niveau de l’électrode 1, les molécules de dihydrogčne H2 , provenant d’un réservoir, sont oxydées en ions H+ , qui se déplacent dans la solution électrolytique. Au niveau de l’électrode 2, des électrons, des ions hydrogčne H+ de l’électrolyte et des molécules de dioxygčne O2 , provenant de l’air ambiant, se combinent pour donner de l’eau. Données :couples oxydant/réducteur : H+ (aq)/H2 (g) et O2 (g)/H2O ( l ) Volume molaire d’un gaz Vm dans les conditions d’utilisation de cette pile : Vm = 24 L/mol. H2
(g) = 2 H+ (aq) +
2e-. Préciser le sens
de circulation du courant électrique dans le
circuit extérieur. Au niveau de l'électrode 1, l'oxydation
de H2 libčre des électrons
: dans le circuit extérieur, les
électrons vont de l'électrode 1 vers
l'électrode 2. Le sens conventionnel du courant
électrique est en sens contraire du sens de
déplacement des électrons :
de
l'électrode 2 vers l'électrode
1.
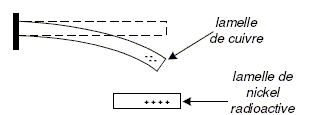
Des scientifiques de l’université Cornell (USA) ont conçu un prototype de pile miniature constituée de deux lamelles superposées, légčrement espacées : celle du dessous est initialement composée de nickel 63 ( 63Ni), un matériau radioactif qui émet des électrons ; celle du dessus est en cuivre. Lorsque des électrons qui s’échappent du nickel atteignent la lamelle de cuivre, elle se charge négativement. Attirée par la lamelle de dessous, dont la charge devient positive, elle se plie, se décharge par contact et revient ŕ l’état initial. L’énergie mécanique de ce mouvement est transformée en énergie électrique ŕ l’aide d’un systčme piézo-électrique qui génčre de l’électricité quand il est déformé. Si le rendement électrique d’un tel dispositif est faible, son encombrement est particuličrement réduit (les scientifiques espčrent parvenir ŕ construire une pile de 1 cm3) et sa durée de fonctionnement devrait dépasser plusieurs dizaines d’années. D’aprčs un extrait de «Ordinateur individuel
Quel est le type de transformation radioactive du nickel 63 ? Emission d'électron, donc radioactivité de type b-. Compléter l'équation de désintégration radioactive du nickel 63 en identifiant le noyau formé. 6328Ni ---> AZX +0-1e . Conservation de la charge : 28 = Z-1 d'oů Z = 29 : on identifie X ŕ Cu. Conservation du nombre de nucléons : 63=A+0. 6328Ni ---> 6329Cu +0-1e . On note N(t) le nombre de noyaux radioactifs de nickel présents dans la pile ŕ l’instant t et N0 le nombre de ces noyaux présents ŕ un instant t0 = 0 pris comme origine des dates. La constante radioactive du nickel 63 vaut l = 6,9 × 10 - 3 an- 1. Rappeler la loi de décroissance radioactive N(t) en fonction N0 et l. N(t) = N0 e(-lt). Donner la définition du temps de demi-vie t1/2 d’une source radioactive. Durée au bout de laquelle l'activité initiale a été divisée par deux. Durée au bout de laquelle le nombre de noyaux initiaux est divisé par deux. Montrer que t˝ = ln2 / l. d'une part : N(t) = N0.e-l.t ; d'autre part ŕ t=t˝ , N(t˝) = ˝ N0 = N0.e-l.t˝ ; d'oů ˝ = e-l.t˝ ; ln ˝ = -l.t˝ ; ln2 =l.t˝ ; t˝ = ln2 /l Calculer t˝. Aide au calcul : ln2 = 0,69. t˝ = 6,9 10-1 / 6,9 × 10 - 3 =1/10-2 = 1,0 102 ans. Ce résultat est-il en accord avec celui indiqué dans le document ? La source radioactive devient pratiquement inactive au bout d'environ 8 demi-vie soit environ 800 ans. "sa durée de fonctionnement devrait dépasser plusieurs dizaines d’années" : donc accord avec le texte.
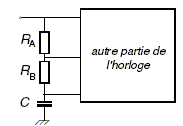
Principe de l’horloge d’un appareil nomade. Tous les appareils nomades ont besoin d’une horloge (alimentée par une pile). Dans ce paragraphe on va étudier l’évolution temporelle d’un circuit (R,C) qui fait partie de l’horloge.
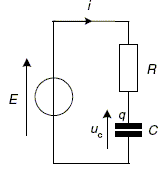
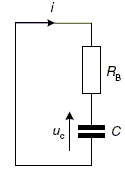
Dans un premier temps le condensateur, initialement décharge, de capacité C est chargé ŕ travers les conducteurs ohmiques de résistances RA et RB. On note E la tension aux bornes du générateur. Lors de cette étape, on considčre que les conducteurs ohmiques et le condensateur de capacité C = 22 mF sont branches en série. Le circuit équivaut alors ŕ : ( avec R = RA + RB = 66 kW ).
Donner la relation qui lie l’intensité instantanée i(t) du courant électrique qui circule dans le dipôle (R,C) ŕ la charge instantanée q(t) de l’armature du condensateur notée sur la figure, puis ŕ la tension uC(t). i(t) = dq(t) /dt ; q(t) = C uC(t) d'oů : i(t) = C duC(t) /dt. Déterminer, en justifiant la réponse, l’équation différentielle qui régit l’évolution de la tension uC(t) aux bornes du condensateur au cours de sa charge. Additivité des tensions : E = Ri + uC ; or i = CduC /dt. par suite E= RCduC/dt + uC. Dčs que la tension uC(t) aux bornes du condensateur atteint une valeur de référence Umax=2E/3, le reste de l’horloge change d’état électrique et fait décharger le condensateur ŕ travers le seul conducteur ohmique de résistance RB = 33 kW . Le circuit équivaut alors ŕ celui qui est représenté :
Déterminer, en justifiant la réponse, l’équation différentielle qui régit l’évolution de la tension uC(t) aux bornes du condensateur au cours de sa décharge dans le conducteur ohmique de résistance RB. Additivité des tensions : 0 = RBi + uC ; or i = CduC /dt. par suite 0= RBCduC/dt + uC.
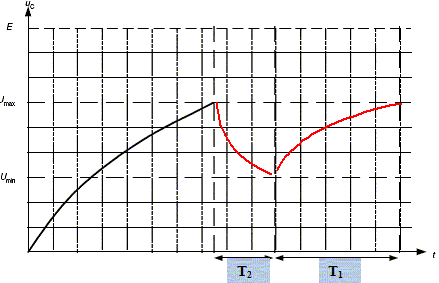
Dčs que la tension uC(t) aux bornes du condensateur atteint une autre valeur de référenceUmin=E/3, le reste de l’horloge change d’état et impose un nouveau cycle de charge du condensateur puis de décharge, etc. La durée de charge du condensateur, entre Umin et Umax, est notée T1 et celle de la décharge, jusqu’ŕ Umin, notée T2. Sachant que les durées de charge et de décharge sont proportionnelles aux constantes de temps du circuit, expliquer, sans calcul, pourquoi la valeur de T1 est supérieure ŕ celle de T2. T1 est proportionnelle ŕ t1=(RA+RB)C ; T2 est proportionnelle ŕ t2=RBC ; RA+RB est supérieur ŕ RB, donc T1 est supérieur ŕ T2. Compléter, l’allure générale de l’évolution au cours du temps de la tension uC(t) lors des différentes phases de charge et de décharge.
|
||||||||
|
|
||||||||
|
|