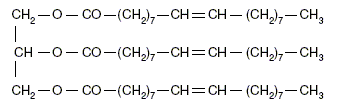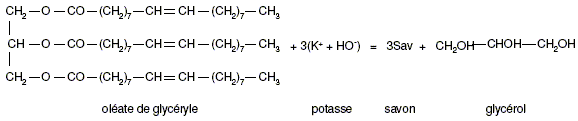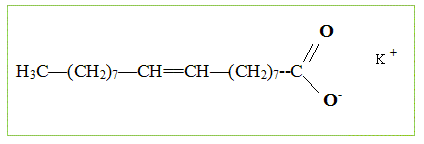|
Histoire
de savons :
bac S France septembre
2008. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
Le savon tire son nom du premier centre de fabrication : Savona, port ligure ouvert sur le golfe de GÍnes. En 1779, William Scheele identifie le glycťrol, alors qu’il saponifiait divers corps gras. ņ partir de 1809, EugŤne Chevreul entreprend une ťtude approfondie des corps gras ; il identifie les principales matiŤres grasses et interprŤte la saponification comme une rťaction chimique. La formule brute du glycťrol est ťtablie en 1836 par Jules Pelouze ; en 1859, Adolphe Wurtz dťcouvre ę la sťrie des glycols Ľ (diols) et en 1873, Charles Friedel fait la synthŤse du glycťrol. La rťvolution industrielle dťveloppe les besoins en savon, qui cesse d’Ítre un produit de luxe et devient un produit de premiŤre nťcessitť. D’aprŤs un site Internet (1) Le texte utilise l’expression ę lessive de cendres et de chaux Ľ pour nommer une solution aqueuse contenant de l’ hydroxyde de potassium et de calcium L’objectif de l’ exercice est
d’ťtudier diffťrentes ťtapes de la
fabrication d’un savon au laboratoire et quelques
propriťtťs des savons.
Les parties 1, 2 et 3 de cet exercice sont
indťpendantes. Fabrication du savon. Le principal constituant de la graisse de boeuf est l’olťate de glycťryle (ou olťine). On rťalise la saponification par une solution d’hydroxyde de potassium (K + + HO- ) d’une huile que l’on considŤrera comme constituťe exclusivement d’olťine, de formule semi-dťveloppťe :
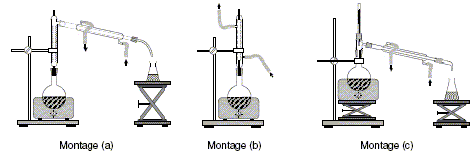
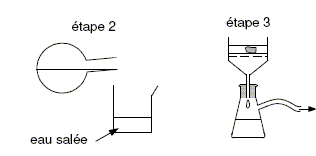
AprŤs la synthŤse, on rťalise les deux ťtapes suivantes dťcrites sur la figure ci-dessous :
Justifier, ŗ l’aide du tableau des donnťes, l’utilisation d’eau salťe dans l’ťtape 2. Le savon est peu soluble dans l'eau salťe : il va donc prťcipiter sous forme d'un solide. Filtration
sous vide : Le savon est rťcupťrť plus
rapidement ; le savon est plus sec que dans le cas
d'une filtration simple. De plus les
impuretťs solubles dans le solvant sont
ťliminťes dans le filtrat
(liquide). …crire une formule semi-dťveloppťe du savon notť Sav dans l’ťquation.
Sachant que l’hydroxyde de potassium a ťtť introduit en excŤs, calculer la quantitť de matiŤre maximale de savon nSav que l’on peut obtenir lors de la saponification de 884 kg de cette huile vťgťtale. Quantitť de matiŤre d'huile : n (mol) = m(g) / M g/mol) =884 103 / 884 = 1,00 103 mol. D'aprŤs les coefficients stoechiomťtriques : nSav = 3 nhuile = 3,00 103 mol. Montrer que la masse maximale de savon mSav susceptible d’Ítre obtenue est 960 kg. mSav = nSav MSav =3,00 103*320= 960 103 g = 960 kg. Quelle est la masse de savon rťellement obtenue mr si le rendement de l’expťrience est ťgal ŗ 90% ? Aide aux calculs : 9,6/9 = 3,1 ; 9,6*0,9 ~ 8,6 ; 90/9,6~9,4 960*0,9 = 9,6*0,9*100 ~ 8,6*100~ 860 kg.
Questions relatives ŗ l'histoire des savons. Le texte utilise les termes ę savons Ľ et ę graisses de mouton, de boeuf ou de chŤvre Ľ. Attribuer ŗ chacun de ces deux termes la famille chimique correspondante choisie parmi les trois suivantes : triester d’acides gras, acide carboxylique, carboxylate de potassium. "savons" : carboxylate de potassium " graisses de mouton, de boeuf ou de chŤvre" : triester d'acide gras. Quel facteur cinťtique a permis d’amťliorer la recette de Galien au XVŤme siŤcle ? "La fabrication du savon, par ťbullition d’un corps gras et d’une base, ne se dťveloppera qu’au XVŤme siŤcle" Le facteur cinťtique est la tempťrature. Le glycol est le plus simple des diols. On donne sa formule semi-dťveloppťe : CH2OH – CH2OH Recopier cette formule, entourer le (ou les) groupe(s) caractťristique(s) et nommer la fonction correspondante. Deux fonctions alcools primaires – CH2OH sont prťsentes.
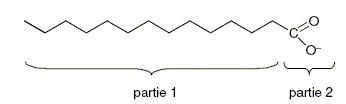
Le pouvoir nettoyant du savon. Un ion carboxylate peut-Ítre schťmatisť par :
Identifier la partie hydrophile et la partie hydrophobe de l’ion. La partie 1, longue chaine carbonťe est hydrophobe ; la partie 2, portant une charge ťlectrique, est hydrophile ( amie de l'eau) Que reprťsente la partie 1 de l’ion carboxylate ? CH3-(CH2)7-CH=CH-(CH2)7-.
|
||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||
|
|