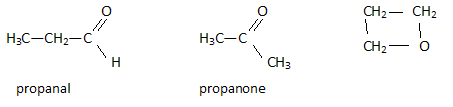|
Prťparateur en chimie : concours ITRF Poitiers 2008.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
K : 39,1 ; H : 1,0 ; Mn : 54,9 ; Na : 23,0 ; O : 16,0 ; Mg : 24,3 Donner la formule brute du permanganate de potassium et calculer sa masse molaire : KMnO4 ; M = 39,1 + 54,9 + 4*16 = 158 g/mol. Quelle quantitť doit-on peser pour prťparer 500 mL de solution ŗ 0,5 mol/L ? Quantitť de matiŤre (mol) = concentration (mol/L) * volume de la solution ( L) n = C V = 0,5*0,5 = 0,25 mol. Masse (g) = quantitť de matiŤre (mol) * masse molaire ( g/mol) = 0,25*158 = 39,5 g. A partir de cette solution mŤre, on rťalise une dilution pour obtenir une solution ŗ 10 mmol/L. Quel volume de solution mŤre doit-on prťlever pour un volume final de 100 mL ? 10 mmol/L = 0,01 mol/L ; facteur de dilution : F = concentration mŤre / concentration fille = 0,5/0,01 = 50. Volume de solution mŤre ŗ prťlever : volume final / F = 100 / 50 = 2 mL. Pour l'ensemble de cette prťparation, vous disposez du matťriel suivant : pipette jaugťe, pipette graduťe, burette, propipette, becher, fiole jaugťe, ťprouvette, ballon rodť. Lequel choisir ? La solution mŤre est dans un bťcher ; la solution mŤre est prťlevťe ŗ l'aide d'une pipette jaugťe + propipette. La solution fille est dans une fiole jaugťe de 100 mL. NaOH ; MM=40 ; solution
ŗ 32 % ; d=1,35. QŤuel volume de
solution commerciale d'hydroxyde de sodium
devez-vous prťlever pour prťparer 1 L
d'une solution diluťe ŗ 0,5
mol/L ? Un litre de solution commerciale a une masse de
1,35 kg ( 1350 g). Masse d'hydroxyde de sodium pur dans 1 L de
solution commerciale : 1,35*0,32 = 0,432 kg = 432
g Quantitť de matiŤre (mol) = masse
(g) / masse molaire (g/mol) = 432/40 =120,8 mol Concentration de la solution mŤre : 10,8
mol/L. Facteur de dilution F = concentration
mŤre / concentration fille ( sol
diluťe) = 10,8/0,5 = 21,6. Volume ŗ prťlever : volume final /
F = 1 /21,6 =0,0463 L =
46,3
mL.
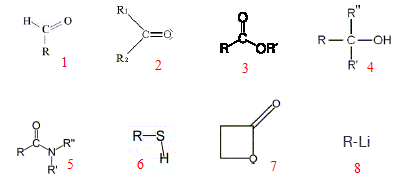
MnO4- + 8 H+ +5 e- = Mn2+ + 4 H2O. 2 NaOH + H2SO4 = Na2SO4 + 2 H2O. C4H10 + 13,5 O2 = 4 CO2 + 5 H2O. CaCO3 + 2 HCl = CO2(g) + CaCl2 + H2O. Nommer les fonctions suivantes.
1 : aldehyde ; 2 : cťtone ; 3 : ester ; 4 : alcool tertiaire ; 5 : amide ; 6 : thiol ; 7 : lactone ; 8 : organolithien.
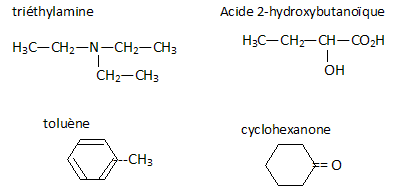
Donner les formules semi-dťveloppťes des produits suivants :
L'analyse ťlťmentaire d'un produit organique donne C3H6O. C : 12,01 ; H :1,01 ; O : 15,99 g/mol. Dťterminer la masse molaire. M = 3*12,01 + 6*1,01 + 15,99 =58,08 g/mol. Dťterminer la composition centťsimale en masse de ce composť. Proportion de carbone C : 3*12,01 / 58,08 *100 =62,04 %. Proportion d'ťlťment hydrogŤne : 6*1,01 / 58,08 *100 =10,43 %. Proportion d'ťlťment oxygŤne : 15,99 / 58,08 *100 =27,53 %. Donner la reprťsentation de trois isomŤres possibles.
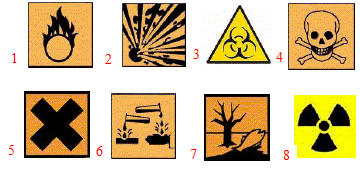
Quel code de couleur est associť aux gaz suivants.
trompe ŗ eau ; pompe ŗ membrane ; pompe ŗ diffusion. 10-3 mbar = 10-3 hpa. Le vide prrimaire ( 1000 ŗ 1 hPa) est obtenu ŗ l'aide de pompe ŗ palettes. Le vide secondaire ( 1 ŗ 10-7 hPa) est obtenu ŗ l'aide de pompe turbomolťculaire, de pompe ŗ diffusion d’huile. Quelle est la plage d'unitť de pH d'utilisation d'une ťlectrode combinťe ? 0 ŗ 7 ; 7 ŗ 14 ; 0 ŗ 14. Quelle solution utilisez-vous pour un stockage prolongť de cette derniŤre ? KCl ŗ 3 mol/L. Faire l'association entre techniques et matťriel.
- l'acťtone de lavage ( non ); une solution aqueuse de chlorure de potassium ( oui ) ; du toluŤne ( non ) ; une solution acide diluťe ( 10-3 mol/L ( oui ) ; une solution de sel de chrome ( non ). Pour diluer un acide concentrť on procŤde en versant l'eau dans l'acide : non, verser l'acide concentrť dans l'eau.
Peut-on stocker dans la mÍme armoire ? - ťther de pťtrole et chloroforme non solvant inflammable et solvant chlorť - solution de soude et du sodium non le sodium doit Ítre maintenu en absence d'humiditť - acide nitrique et potasse : non rťaction acide base exothermique - peroxyde d'hydrogŤne et aluminium : non rťaction oxydorťduction exothermique - acide oxalique et acide chlorhydrique oui. Citez quatre ťquipements collectifs de sťcuritť disponibles dans une salle de TP de chimie. Extincteurs, douche, couverture, ventilation des salles. Equipements de Protection Individuelle : blouse, gants, lunettes et chaussures de sťcuritť.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
c |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|