|
QCM acide base : concours blanc kiné d'aprčs P Chantant
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées ŕ vos centres
d’intéręts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
A- L'ion hydrogénosulfite HSO3- (aq) est une espčce chimique ampholyte. Vrai. H2SO3 /HSO3- (aq) : HSO3- (aq) joue le rôle de base. HSO3- (aq) / SO32- : HSO3- (aq) joue le rôle d'acide. Un ampholyte ( ou amphotčre) est une espčce pouvant se comporter ŕ la fois comme un acide et une base. B- En solution aqueuse, le chlorure d'hydrogčne est un acide fort plus fort que l'acide nitrique. Faux. L'acide le plus fort existant dans l'eau est H3O+. Tout acide plus fort réagit avec H2O pour former H3O+. On dit " il y a nivellement de l'acidité par le solvant, l'eau". C- L'ion H+ est un acide. Faux. L'ion H+ hydraté est un acide. H+ est un proton. Lors d'une réaction acide base, il y a transfert d'un proton H+ de la forme acide d'un couple acide / base ŕ la forme base de l'autre couple. D- L'acide aminoéthanoďque H2N- CH2-COOH est l'acide conjugué de l'ion +H3N- CH2-COOH. Faux. +H3N-
CH2-COOH /
H2N- CH2-COOH ;
H2N- CH2-COOH joue le
rôle de base.
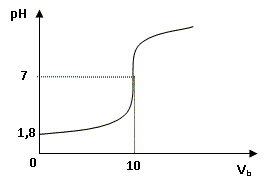
A- Le pH théorique du mélange final ŕ l'équilibre vaut 7 ŕ 25°C. Vrai.
Les réactifs se trouvent en proportions stoechiométriques. la solution finale est une solution de chlorure de potassium, milieu neutre de pH=7. B- Dans le mélange [Cl-]eq = [K+]eq = 2 mmol/L. Vrai. Les ions chlorure et potassium sont spectateurs : n(Cl-) = n(K+) = 0,2 mmol dans 0,1 L. [Cl-]q = [K+] =0,2/0,1 = 2 mmol/L. C- Dans le mélange final ŕ l'équilibre il n'y a plus d'ions hydronium et d'ions hydroxydes. Faux. A pH=7 il y a autant d'ion oxonium ( hydronium ) que d'ion hydroxyde. D- Lors du mélange la seule réaction est l'autoprotolyse. Faux. couples acide / base mis en présence : H3O+ /H2O et H2O / HO-. La réaction prépondérante est : HO- + H3O+ = 2 H2O.
Volume de la solution V = 0,2 L ; [HO-] =xfin / V soit xfin = [HO-] V = 2,5 10-3 *0,2 =5,0 10-4 mol. C- Lors de la réaction entre l'ammoniac gazeux NH3 et l'eau, l'eau est l'acide. Vrai. Couple acide /base : NH4+/ NH3 et H2O /HO- NH3 + H2O =NH4+ +HO-. D- La réaction de l'ammoniac sur l'eau est : NH3 (g)+ H2O =NH4+ +HO-.Vrai.
On dispose de nitrate de fer III solide. On veut préparer 250 mL d'une solution aqueuse de nitrate de fer III telle que la concentration des ions nitrate soit égale ŕ 0,6 mol/L. Le sulfate de fer est totalement soluble. La masse de nitrate de fer III ŕ dissoudre est égale ŕ : A : 36,3 g B : 108,9 g C : 12,1 g D : 48,4 g Masse molaire en g/mol : Fe = 56 N = 14 O = 16. Dissolution du solide : Fe(NO3)3(s) = Fe3+(aq) + 3NO3-(aq). (1) n(NO3-) = 0,6*0,25 =0,15 mol. D'aprčs les nombres stoechiométriques de (1) : n(Fe(NO3)3(s) ) = 0,15/3 = 0,05 mol. Masse molaire Fe(NO3)3 : M= 56+3(14+3*16) = 242 g/mol. m = n M = 0,05*242 = 12,1 g.
Le phénol C6H5OH est un acide dont la solution aqueuse appelée eau phéniquée, possčde des propriétés antiseptiques. Sa solubilité dans l'eau est de 9,4 g.L-1. Le pH d'une solution saturée de phénol est égal ŕ 5,0. A- La concentration molaire en soluté apporté d'une solution saturée de phénol est égale ŕ 0,10 mol.L-1. Vrai. Masse molaire du phénol : M= 6*12+6+16 = 94 g/mol. 9,4 / 94 = 0,10 mol/L. B- La forme basique du couple dont le phénol est la forme acide s'écrit C6H5O - . Vrai. C6H5OH = C6H5O - +H+. C- Le taux d'avancement de la réaction du phénol dans l'eau est supérieur ŕ 10 %. Faux. Pour un litre de solution : xfin = 10-pH = 10-5 mol ; xmax = 0,1 mol taux d'avancement final : xfin / xmax =10-5 /0,1 = 10-4. D- La réaction entre le phénol et l'eau est totale. Faux. Le taux d'avancement final est trčs inférieur ŕ 1 : la réaction est trčs limitée.
Ŕ 37°C, le produit ionique de l'eau est Ke = 2,5 .10-14. A 25°C, pKe = 14. A- La valeur du produit ionique de l'eau augmente avec la température. Vrai. B- Ŕ 37°C, la salive de pH= 6,8 est neutre. Vrai. [H3O+] [HO-] =2,5 10-14; solution électriquement neutre [H3O+]= [HO-] [H3O+]= (2,5 10-14)˝ = 1,6 10-7 ; le pH d'un milieu neutre, ŕ 37°C vaut -log 1,6 10-7 =6,8. C- Dans une solution aqueuse d'hydroxyde de potassium telle que [HO- ] =2,5 10-3 mol/L , la concentration en ions oxonium ŕ 37°C est égale ŕ 1,0.10-11 mol/L. Vrai. [H3O+] [HO-] =2,5 10-14 ; [H3O+]= 2,5 10-14 / 2,5 10-3 =1,0 10-11 mol/L. D- En milieu aqueux, la réaction 2H2O(l) = HO-(aq)+ H3O+(aq) n'a lieu que dans l'eau pure de pH égal ŕ 7. Faux. Autoprotolyse de l'eau : cette
réaction a lieu dans toute solution aqueuse.
Quel volume ( en mL) de la solution commerciale doit-on prélever pour préparer 3 L de solution d'acide chlorhydrique ŕ 0,02 mol/L. A : 5,1 ; B : 26 ; C : 65 ; D : 85 ; Masse de 1 L de solution : 1,19 kg = 1190 g ; masse d'acide pur : 1190*0,36 =428,4 g quantité de matičre d'acide dans un litre ( concentration) : 428,4/36,5 =11,7 mol/L Facteur de dilution F = 11,7 / 0,02 = 587. Volume de solution mčre ŕ prélever pour obtenir 1 L de solution fille ŕ 0,02 mol/L : 1000 / 587 =1,7 mL soit 1,7*3
=5,1
mL pour obtenir 3 L de
solution diluée ŕ 0,02 mol/L.
lNa+ = 5. 10-3 ; lCl- = 7,6 10-3 ; lHO- = 19,8 .10-3 ; lH3O+ = 34,9 .10-3. La conductivité d'un mélange de 2 litres de soude 10-4 mol /L et de 10 mL d'acide chlorhydrique 0,02 mol.L-1 vaut environ : A- la conductivité d'une solution aqueuse de chlorure de sodium de concentration voisine de 10-3 mol/L . Faux.
n(Na+) = n(Cl-) = 2 10-4 mol dans 2,01 L ; [Na+] =[Cl-]=2 10-4 /2,01 ~ 10-4 mol/L. B- 1,26 mS. m-1 . Vrai. [Na+] =[Cl-] =10-4 mol/L = 0,1 mol m-3. Conductivité de la solution : s = lNa+[Na+] +lCl-[Cl-] = (5 +7,6)10-3*0,1 = 1,26 10-3 S m-1 = 1,26 mS m-1. C- 0,126 mS.cm-1 . Faux. 1,26 mS m-1= 1,26 /100 mS cm-1 = 1,26 10-2 mS cm-1. D- 12,6.10-3 mS.m-1. Faux.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|