|
|
|||||||||||||||||||||||||
|
1 bobine inductive |
corrigé |
||||||||||||||||||||||||
|
mesure directe de la résistance de la bobine (hors circuit) à l'ohmmètre. déterminer l'inductance en réalisant un circuit RLC série et se placer à la résonance d'intensité . On visualise à l'oscilloscope la tension aux bornes du dipole et aux bornes de la résistance R0 : à la résonance ces deux sinusoïdes sont en phase ( non décalées) . Lire la fréquence sur le GBF. la relation LC0(2pf)²=1 donne L la capacité étant connue.
|
|||||||||||||||||||||||||
|
choix d'une résistance |
On prendra comme valeur de la tension de saturation du composant TL 081 : Vsat+=12V et Vsat- = -12V. 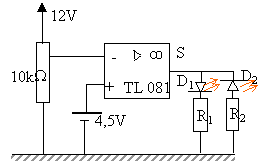
données : série E12 (10%) : 1 ; 1,2 ; 1,5 ; 1,8 ;2,2 ; 2,7 ; 3,3 ; 3,9 ; 4,7 ; 5,6 ; 6,8 ; 8,2 .
corrigé |
||||||||||||||||||||||||
|
L'A.O fonctionne en saturation : suivant la position du curseur du rhéostat à l'entrée la tension de sortie est +12 ou -12V. L'une ou l'autre des deux diodes électroluminescentes va éclairer. La tension de sortie USmasse est égale en valeur absolue à 12V. C'est à dire 12-1,8 = 10,2 V aux bornes du résistor R1 ou R2. L'un ou l'autre de ces résistor en série avec D1 ou D2 est traversé par un courant d'intensité 11 mA 10,2= R1 *0,011 d'où R1 =927 ohms puissance à dissipée : 10,2*0,011 = 0,11 W On choisit 1 kW et une puissance de ¼W
le premier trait marron indique : 1 le deuxième trait orangé indique multiplier par 1000 le troisième trait argent concerne la précision 10%
|
|||||||||||||||||||||||||
|
tests d'ions |
Compléter le tableau suivant :
corrigé |
||||||||||||||||||||||||
En présence de chlorure de baryum, les ions sulfates donnent un solide blanc de sulfate de baryum BaSO4. En présence de carbonate de sodium, l'ion calcium donne un solide blanc de carbonate de calcium CaCO3. En milieu acide , l'ion hydrogénocarbonate conduit au dégagement de CO2 qui trouble l'eau de chaux.
|
|||||||||||||||||||||||||
|
dosage des sucres dans une limonade |
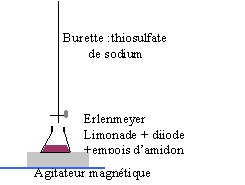
La limonade est une boisson gazeuse qui contient du dioxyde de carbone, du glucose, du saccharose, de l'acide citrique et un arôme naturel de citron. A l'obscurité et à froid, seul le glucose peut être oxydé par les ions iodates IO3- formé lors de la dismutation du diiode en milieu basique. Pour déterminer la concentration en saccharose de la limonade il sera nécessaire d'en réaliser l'hydrolyse en milieu acide. expérience 1 : Dans 5 mL de limonade dégazée, on ajoute 20 mL de diiode de concentration C0=0,05 mol/L et 2,5 mL de soude à 2,5 mol /L. On laisse reposer le mélange à l'obscurité pendant 30 min. On ajoute ensuite 8 mL d'acide chlorhydrique à 2 mol/L et on dose le diiode réapparu par une solution de thiosulfate de sodium à 0,1 mol/L. On observe une décoloration totale du mélange pour un volume de 14,4 mL de thiosulfate de sodium ajouté. expérience 2 : Dans un erlenmeyer de 125 mL on ajoute 5 mL de limonade dégazée, 5 mL d'acide chlorhydrique à 2 mol/L et on chauffe à 80° pendant 20 min. Après refroidissement, on ajoute 20 mL de diiode de concentration C0=0,05 mol/L et 9 mL de soude à 2,5 mol /L.On laisse reposer le mélange à l'obscurité pendant 30 min. On ajoute ensuite 8 mL d'acide chlorhydrique à 2 mol/L et on dose le diiode réapparu par une solution de thiosulfate de sodium à 0,1 mol/L. On observe une décoloration totale du mélange pour un volume de 7,9 mL de thiosulfate de sodium ajouté. données : thiosulfate de sodium à 5 moléculesd'eau : Na2S2O3, 5H2O ,M= 248,17 g/mol hydroxyde de sodium : 40 g/mol; lessive de soude à 35% en masse ; d=1,38.
corrigé |
||||||||||||||||||||||||
|
le diiode en présence d'empois d'amidon donne une couleur violette presque noire.
peser 24,8 g de thiosulfate de sodium, dissoudre dans l'eau distillée, placer dans une fiole jaugée de 1L, compléter avec de l'eau distillée jusqu'au trait de jauge. la soude est à 2,5 mol/L. Un litre de lessive de soude a une masse de 1380 g et contient : 1380*0,35 = 483 g de soude pure soit 483 /40 = 12,07 mol/L facteur de dilution : 12,07 / 2,5 = 4,83 volume de lessive de soude à prélever : 500/4,83 = 103,5 L mesurer 103 mL de lessive de soude avec une éprouvette graduée; placer dans une fiole jaugée de 500 mL; compléter à l'eau distillée. |