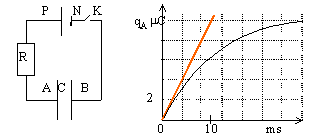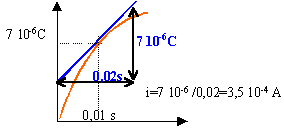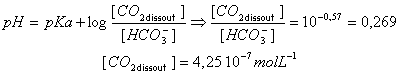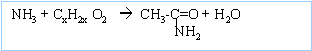|
|
|
|
charge d'un condensateur |
|
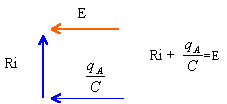
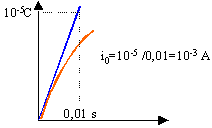
au début de la charge , qA est peu différent de zéro. En conséquence i0=E/R. D'après la courbe, la valeur finale de la charge est 10-5 C. Or qA=CUAB--> UAB=10-5 / 2 10-6 = 5V. intensité i0 : pente de la tangente à la courbe à t=0.
d'où R= E/i0 =5 kW. à la date t=0,01 s :
U= 7 10-6 / 2 10-6 = 3,5 V.
|
|
|
réactions nucléaires |
Le noyau de Thorium Th (A=232 et Z=90) bombardé par des neutrons, peut capter l'un d'entre eux pour donner un isotope du thorium qui se trouve dans un état excité. Cet isotope revient ensuite à son état fondamental.
corrigé |

Z augmente de une unité à chaque réaction. Un neutron du noyau se transforme en proton avec émission d'un électron radioactivité de type b-.
variation de masse : 233,0395-(229,0316+4,0026)=5,3 10-3 u 5,310-3 * 931,5 = 4,94 MeV 4,94 *1,6 10-13 = 7,9 10-13 J vitesse de la particule alpha : 7,9 10-13 = 0,5 *(4,0026*1,66 10-27 ) v² (masse en kg) v=1,54 107 m/s.
|
|
|
réactions acide base |
CO2 dissout + H2O en équilibre avec HCO3- + H3O+ Le pKa du couple auquel appartient CO2 dissout vaut 6,37.
corrigé |
|
[H3O+]=10-5,8 =1,58 10-6 mol L-1. produit ionique de l'eau : [OH-]=10-14 / 1,58 10-6 =6,33 10-9 mol L-1. solution électriquemet neutre : [OH-]+[HCO3-]=[H3O+] [HCO3-] voisin de [H3O+]
conservation de l'élément carbone : [CO2 dissout]+[HCO3-] =(1,58+0,425)10-6=2 10-6 mol L-1. soit dans 5 L :10-5 mol ou 10-5 *25= 0,25 mL
|
|
|
réactions organiques |
Déterminer en justifiant les réponses les formules semi dveloppées et les noms des composés A, B, C et D. corrigé |

n+x=5
éthanamide (x=2 donc n=3) et B est l'acide éthanoïque. l'oxydation d'un alcool primaire donne un aldehyde qui rosit le réactif de Schiff et réagit avec la DNPH. cet alcool compte en plus trois carbone A est le propan-1-ol. C est le propanal CH3-CH2-CHO D est un chlorure d'acyle comptant deux carbones CH3-COCl, chlorure d'éthanoyle.
retour - menu |